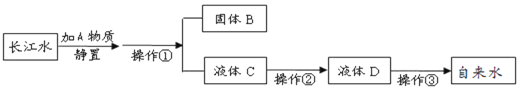
题目内容
【题目】图A是钠元素在元素周期周期表中的信息,B、C、D分别是三种元素的原子结构示意图,根据题中信息回答下列问题:
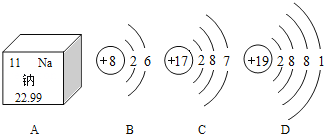
(1)请画出11号元素原子结构示意图_____,化学反应中该原子比较容易_____(填“得到”或“失去”)电子变成离子,离子符号为_____.
(2)如图A所示:钠原子的核电荷数是_____,钠原子的相对原子质量是_____.
(3)图B、C、D中表示金属元素的是_____(填序号).
(4)图C和D所属元素形成的化合物的化学式为_____.
【答案】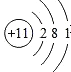 失去 Na+ 11 22.99 D KCl
失去 Na+ 11 22.99 D KCl
【解析】
(1)11号元素质子数为11,核外电子数为1,有3个电子层,最外层有1个电子,原子结构示意图: ,易失去1个电子变成离子,离子符号为Na+;
,易失去1个电子变成离子,离子符号为Na+;
(2)钠原子的核电荷数是11,钠原子的相对原子质量是22.99;
(3)B是氧元素,C是氯元素,D是钾元素;
(4)氯原子最外层有7个电子,易得一个电子,而显﹣1价;钾原子最外层有1个电子,易失去一个电子而显+1价,化学式为:KCl。

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案【题目】某化学活动小组合作学习氢氧化钠和氢氧化钙的相关知识。如表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
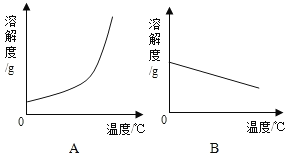
(1)依据上表数据,绘制了Ca(OH)2和NaOH的溶解度曲线,图中能表示NaOH溶解度曲线的是_____(填“A”或“B”)。
(2)将一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入适量氢氧化钙②升高温度③降低温度④加入水⑤蒸发水后再恢复到原温度⑥加入适量生石灰。
其中措施在原理上正确的是_____(填字母)
A ②④⑥ B ③④ C ①②⑤⑥ D ①②⑤
(3)20℃时,191g饱和NaOH溶液,蒸发10g水后,再恢复到20℃,可析出NaOH固体。这时溶液的质量分数为_____
(4)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH_____(填“偏大”或“偏小”“不受影响”)。
(5)可鉴别氢氧化钠溶液和澄清石灰水的一个化学反应方程式为_____。