题目内容
【题目】如图是初中化学中的一些重要实验。请回答下列问题:
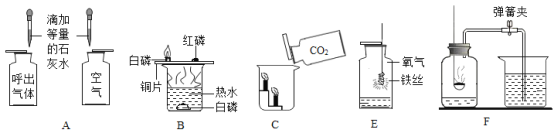
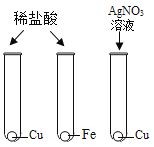
(1)A实验的目的是______。
(2)B实验中,通过对比铜片上的白磷和红磷,得出燃烧的条件是______。
(3)由C实验得出CO2的化学性质是______。
(4)D实验中水的作用是______。
(5)E实验的原理是______。
【答案】比较吸入气体和呼出气体中二氧化碳的含量 温度达到着火点 不燃烧,不支持燃烧 防止熔化物炸裂瓶底 红磷燃烧消耗氧气,使瓶内压强小于瓶外压强,形成倒吸现象,吸入水的体积等于消耗氧气体积
【解析】
红磷燃烧生成五氧化二磷,铁在氧气中点燃生成四氧化三铁。
(1)由图示实验可知,分别呼出气体和空气中滴加等量的石灰水,根据变浑浊的情况来判断气体中二氧化碳的含量,故A实验的目的是比较吸入气体和呼出气体中二氧化碳的含量。
(2)铜片上的白磷在热水的温度下达到着火点,能够燃烧;红磷由于着火点高,热水不能使其达到着火点,所以不能燃烧。通过对比铜片上红磷和白磷的现象,可以得出可燃物燃烧的条件之一为温度需达到可燃物着火点。
(3)将二氧化碳沿着烧杯壁倾倒入烧杯中后会看到蜡烛由下至上依次熄灭,这说明二氧化碳不燃烧,也不支持燃烧(化学性质),且密度比空气大(物理性质)。
(4)铁丝在氧气中的燃烧生成的黑色固体的温度很高,为了防止高温生成物溅落炸裂瓶底,所以在集气瓶内加入少量的水。
(5)用红磷来测定空气中氧气含量的原理是红磷燃烧消耗氧气,使瓶内压强小于瓶外压强,形成倒吸现象,吸入水的体积等于消耗氧气体积。

【题目】某同学进行下图两个实验。
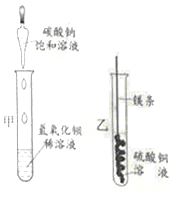
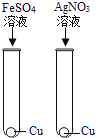
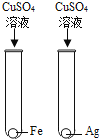
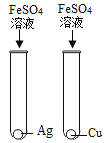
(l)甲实验中反应的化学方程式为____________;
(2)乙实验观察到的现象是___________,溶液由蓝色变成无色。
(3)把甲、乙反应后的溶液倒入同一烧怀,发现有白色沉淀生成。他决定对白色沉淀的成分进行探究。
【查阅资料】硫酸钡不溶于酸。
【提出猜想】 白色沉淀为:Ⅰ._______;Ⅱ.Mg(OH)2和BaSO4;Ⅲ.Mg(OH)2和MgCO3.
【实验方案】
实验操作 | 实验现象与结论 |
过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①若沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化学反应方程式为____________。 ②若______且无气体产生,猜想Ⅱ成立。 ③若沉淀完全溶解,________,猜想Ⅲ成立。 |
【拓展与思考】如果猜想Ⅲ成立,产生此结果的原因是做甲实验时___________;上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是__________________。