题目内容
【题目】某兴趣小组成员小茗在家发现妈妈将拌了“安多夫”粉的肉加入食醋腌制时产生大量气泡,引发了极大兴趣。兴趣小组在查阅资料后得知,“安多夫” 是一种嫩肉粉,其主要成分中含有碳酸氢钠,联想到学过的碳酸钠,与碳酸氢钠仅相差一种氢元素, 于是决定对碳酸钠、碳酸氢钠和酸的反应进行探究。
[提出问题]
碳酸钠、碳酸氢钠和稀盐酸反应产生二氧化碳的速率是否相同?
[设计与实验]
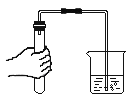
(1)小茗设计的实验如图所示,实验时,两注射器中的稀盐酸应____(填具体操作),观察到图所示两个气球膨胀速度来判断反应的速率。

(2)小红对小茗的实验提出了质疑:
①碳酸钠、碳酸氢钠固体和稀盐酸反应都很剧烈,通过观察很难判断产生气体的快慢;
②______。
她认为,应取含碳元素质量相同的碳酸钠和碳酸氢钠,若碳酸钠的质量仍为0.318g,应称取碳酸氢钠的质量为__g (写出计算过程)
(3)小组同学在老师指导下设计了如图所示的实验。
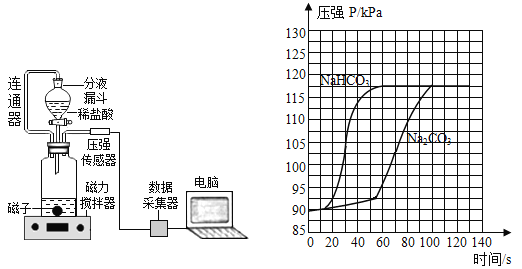
①连通管的作用是________。
②分别取等体积、含碳元素质量相同的碳酸钠和碳酸氢钠稀溶液(各滴2滴酚酞溶液),以及等体积、等浓度的足量稀盐酸进行实验。实验时,溶液颜色变化记录如表,广口瓶内压强随时间变化如图所示
滴入酚酞溶液 | 滴入稀盐酸,溶液颜色变化 | |
碳酸钠溶液 | 红色 | 红色→浅红色→无色 |
碳酸氢钠溶液 | 浅红色 | 淺红色→无色 |
[实验结论]
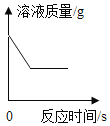
(4)分析图所示的实验数据可得到的结论是:相同条件下,______和稀盐酸反应产生二氧化碳较快。
[交流反思1]
(5)小组同学分析表实验现象和数据,得出碳酸钠和稀盐酸混合产生二氧化碳的反应可以分为两步进行:_____、______。 (请用化学方程式说明)。
[拓展探究]
取等体积、含碳元素质量相同的碳酸钠和碳酸氢钠溶液,分别逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图所示。

[交流反思2]
(6)将图中阴影部分进行叠加,发现两条曲线基本重合,则c点溶液中溶质为______(填化学式)
(7)下列选项中,说法正确的是______。
A 碳酸氢钠俗称小苏打,可以用来治疗胃酸过多
B 图5中b点的溶液中,溶质只有氯化钠
C 等体积、含有碳元素质量相等的碳酸钠和碳酸氢钠溶液中,碳酸钠溶液的碱性较强
D 碳酸氢钠溶液中混有少量碳酸钠,可以加入稀盐酸将碳酸钠除去
【答案】同时注入相同体积的盐酸 产生的二氧化碳量不同 0.252g 平衡压强 NaHCO3 ![]()
![]() NaHCO3、NaCl AC
NaHCO3、NaCl AC
【解析】
碳酸钠与稀盐酸反应生成碳酸氢钠和氯化钠,然后碳酸氢钠与稀盐酸反应生成氯化钠、水和二氧化碳。
[设计与实验]
(1)实验要控制变量,控制盐酸的量相同,故实验时,两注射器中的稀盐酸应同时注入相同体积的盐酸,观察到图所示两个气球膨胀速度来判断反应的速率。
(2)②相同质量的碳酸钠和碳酸氢钠与稀盐酸完全反应时,碳酸氢钠生成的二氧化碳多,故产生的二氧化碳量不同。
碳酸钠的质量仍为0.318g,应称取碳酸氢钠的质量为![]() 。
。
(3)①连通管的作用是平衡压强。
[实验结论]
(4)碳酸氢钠和碳酸钠均与稀盐酸反应生成二氧化碳,由图所示的实验数据可得到的结论是:相同条件下,滴加碳酸氢钠集气瓶中压强变化较大,故NaHCO3和稀盐酸反应产生二氧化碳较快。
[交流反思1]
(5)小组同学分析表实验现象和数据,得出碳酸钠和稀盐酸混合产生二氧化碳的反应可以分为两步进行,分别为碳酸钠和稀盐酸生成碳酸氢钠和氯化钠,碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为![]() 、
、![]() 。
。
[交流反思2]
(6)碳酸钠和稀盐酸生成碳酸氢钠,碳酸氢钠和稀盐酸再反应,将图中阴影部分进行叠加,两条曲线基本重合,c点是碳酸氢钠和稀盐酸反应,碳酸氢钠过量,碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳,则c点溶液中溶质是碳酸氢钠和氯化钠,故化学式为NaHCO3、NaCl。
(7)A、碳酸氢钠俗称小苏打,碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,可以用来治疗胃酸过多,故A正确;
B、图5中b点的溶液的pH小于7,溶液显酸性,稀盐酸过量,溶质有氯化钠和氯化氢,故B不正确;
C、碳酸钠溶液中滴加酚酞试液、稀盐酸,颜色变化是红色→浅红色→无色,碳酸氢钠溶液中滴加酚酞试液、稀盐酸,颜色变化是浅红色→无色,等体积、含有碳元素质量相等的碳酸钠和碳酸氢钠溶液中,碳酸钠溶液的碱性较强,故C正确;
D、碳酸氢钠溶液中混有少量碳酸钠,碳酸氢钠和碳酸钠均与稀盐酸反应生成氯化钠、水和二氧化碳,不能加入稀盐酸将碳酸钠除去,故D不正确。故选AC。