��Ŀ����
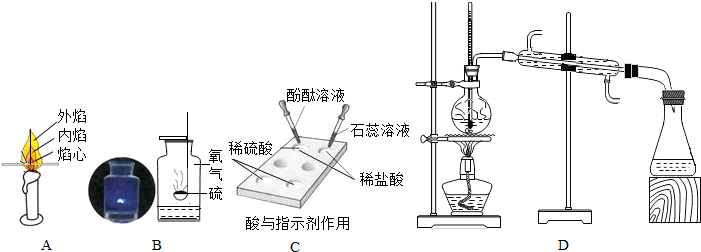
��15�֣������ĸ�ʵ�鶼�ǽ̲��еĻ�ѧʵ�飬����䲢����й�����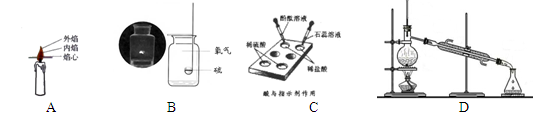 ��1��ʵ��A֤������ȼ�ղ����Ļ��棬�����¶��� ����ߡ��͡��� ��
��1��ʵ��A֤������ȼ�ղ����Ļ��棬�����¶��� ����ߡ��͡��� ����2��ʵ��B������������ȼ��ʵ�飬ƿ��Ԥ�ȼ�ˮ��Ŀ���ǣ� ��С֣ͬѧ�Ը�ʵ�����ҩƷ�Ľ�����ˮ�滻Ϊ���з�̪��Һ�� ��Һ��ʵ��ʱ���ܸ��ôﵽĿ�ģ������ʵ�������Ȥζ�ԡ�
��3��ʵ��C��̽����Ļ�ѧ����ʵ�飬�õ�ΰ�����Թ����ʵ��ĺô��� ��
��4��ʵ��D������ˮ����ȡ���������ˮ�������� ��������ϳ����������³�����������ˮ��������ȴ�����۽Ƕȿ���ˮ���ӵ� ��С�ˡ�
��5������������һ���ܶȴ��ڿ���������ˮ���ж�����ɫ���壬��ͭƬ��Ũ���ᣨHNO3�����ȾͿ����Ƶã�ͬʱ��������ͭ��ˮ��������ع�ʵ������ȡ�����һ��˼·�ͷ���������������⣺
�١���ȫʵ������ȡNO2�Ļ�ѧ����ʽ��
Cu + 4HNO3��Ũ���� Cu(NO3)2 +2 NO2��+ ��
�ڡ���Ӧԭ������ʵ��װ�õ���ơ����ݢٵķ���ʽ��Ҫ��ȡһƿNO2������Ҫѡ������ʵ��װ��A��B��C��D�е�����̨�� �� ��ƿ������������װʵ��װ �ã��ռ������ɲ��� �������б�Ҫ��β������������ʵ��װ�������װ��Ϻ������ ��
�ۡ�����Ԥ����ȡNO2ʱ��ʵ���������ٴ����㣩
�� ���� ��
�ܡ���Ӧ��������Һͨ�� ����������ƣ����Ի������ͭ���塣
��1�� �� ��2�� ���ն�����������Ⱦ���� �� �������ƣ���NaOH��
��3�� ��ԼҩƷ ��4���������ϳ��� �� ���
��5���� 2 H2O �� ����ƿ ���ƾ��� �������ſշ� �� װ��������
�ۢ���Һ����ɫ����ɫ ������������ɫ���� ������ͭƬ���ܽ��ͭƬ����ð���ݵȣ� �� �����ᾧ ����:
���ջ�ѧ����ʽ����д���������ʵ����ʺ���;�ȷ�������ݣ����������Ϣ���з����жϣ����������ʵ�����Ʒ������顢�����뾻��
��3�� ��ԼҩƷ ��4���������ϳ��� �� ���
��5���� 2 H2O �� ����ƿ ���ƾ��� �������ſշ� �� װ��������
�ۢ���Һ����ɫ����ɫ ������������ɫ���� ������ͭƬ���ܽ��ͭƬ����ð���ݵȣ� �� �����ᾧ ����:
���ջ�ѧ����ʽ����д���������ʵ����ʺ���;�ȷ�������ݣ����������Ϣ���з����жϣ����������ʵ�����Ʒ������顢�����뾻��

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
 Cu(NO3)2 +2 NO2��+ ��
Cu(NO3)2 +2 NO2��+ �� 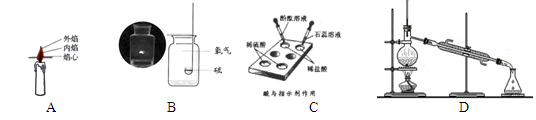 ��1��ʵ��A֤������ȼ�ղ����Ļ��棬�����¶��� ����ߡ��͡��� ��
��1��ʵ��A֤������ȼ�ղ����Ļ��棬�����¶��� ����ߡ��͡��� ��
 Cu��NO3��2+2NO2��+______��
Cu��NO3��2+2NO2��+______��