题目内容
下面四个实验都是教材中的化学实验,请回忆并解决有关问题.
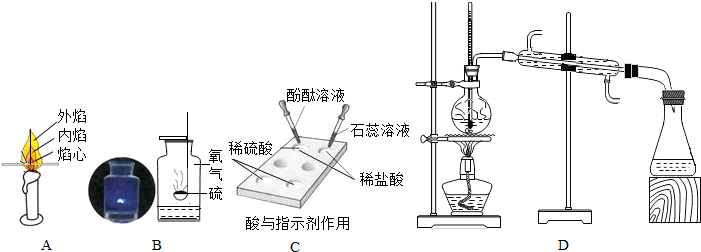
(1)实验A证明蜡烛燃烧产生的火焰,外焰温度最 (填“高”或“低”).
(2)实验B是硫在氧气中燃烧实验,瓶中预先加水的目的是: .小郑同学对该实验进行药品改进,把水替换为滴有酚酞试液的 溶液,实验时既能更好达到目的,又提高实验现象的趣味性.
(3)实验C是探究酸的化学性质实验,用点滴板代替试管完成实验的好处是 .
(4)实验D是蒸馏水的制取,蒸馏过程水的流向是 (填“下入上出”或“上入下出”);高温水蒸气的冷却,从微观角度看是水分子的 减小了.
(5)二氧化氮是一种密度大于空气易溶于水的有毒红棕色气体,用铜片与浓硝酸(HNO3)共微热就可以制得,同时生成硝酸铜和水.现请你回顾实验室制取气体的一般思路和方法,解决下列问题:
①补全实验室制取NO2的化学方程式:Cu+4HNO3(浓)
Cu(NO3)2+2NO2↑+ ;
②反应原理决定实验装置的设计.根据①的方程式,要制取一瓶NO2,至少要选择上面实验装置A、B、C、D中的铁架台、 、 烧瓶等仪器用于组装实验装 置,收集方法可采用 ,并进行必要的尾气处理.整套实验装置设计组装完毕后必须检查 .
③请你预测制取NO2时的实验现象:(至少答两点)Ⅰ: ;Ⅱ: .
④反应后所得溶液通过 (填操作名称)可以获得硝酸铜晶体.

(1)实验A证明蜡烛燃烧产生的火焰,外焰温度最
(2)实验B是硫在氧气中燃烧实验,瓶中预先加水的目的是:
(3)实验C是探究酸的化学性质实验,用点滴板代替试管完成实验的好处是
(4)实验D是蒸馏水的制取,蒸馏过程水的流向是
(5)二氧化氮是一种密度大于空气易溶于水的有毒红棕色气体,用铜片与浓硝酸(HNO3)共微热就可以制得,同时生成硝酸铜和水.现请你回顾实验室制取气体的一般思路和方法,解决下列问题:
①补全实验室制取NO2的化学方程式:Cu+4HNO3(浓)
| ||
②反应原理决定实验装置的设计.根据①的方程式,要制取一瓶NO2,至少要选择上面实验装置A、B、C、D中的铁架台、
③请你预测制取NO2时的实验现象:(至少答两点)Ⅰ:
④反应后所得溶液通过
分析:(1)根据木条烤焦的程度分析;
(2)根据二氧化硫能污染空气以及能与水反应分析;根据氢氧化钠显碱性,能与非金属氧化物反应的性质分析;
(3)根据点滴板的特点分析;
(4)根据冷凝管的冷凝原理分析,从微观的角度的分析水蒸气的变化;
(5)①根据质量守恒定律及反应分析;
②根据制取的原理,分析用到的仪器.根据气体的性质分析收集方法,凡是制取气体的装置都要检查装置的气密性;
③根据铜离子、二氧化氮气体的颜色分析;
④根据结晶的方法分析.
(2)根据二氧化硫能污染空气以及能与水反应分析;根据氢氧化钠显碱性,能与非金属氧化物反应的性质分析;
(3)根据点滴板的特点分析;
(4)根据冷凝管的冷凝原理分析,从微观的角度的分析水蒸气的变化;
(5)①根据质量守恒定律及反应分析;
②根据制取的原理,分析用到的仪器.根据气体的性质分析收集方法,凡是制取气体的装置都要检查装置的气密性;
③根据铜离子、二氧化氮气体的颜色分析;
④根据结晶的方法分析.
解答:解:(1)由于实验A中木条在外焰部分变黑了.所以,外焰温度最高;
(2)由于二氧化硫是对大气由污染的气体.所以,瓶中预先加水的目的是:吸收二氧化硫,避免污染环境;由于氢氧化钠是一种强碱,能与二氧化硫反应,把水替换为能使酚酞试液的变红色的氢氧化钠溶液;
(3)用点滴板代替试管完成实验的好处是节约药品;
(4)水流经过冷凝管后温度会上升,如果水流方向与气流方向相同,那么在冷凝管末端会出现较热的水在冷却较冷的气体这样的情况.如果反过来的话,同一段冷凝管中的水温和气温差别较大,冷却效果更好.高温水蒸气的冷却,从微观角度看是水分子的间隔 减小了
(5)①根据质量守恒定律反应前后原子的种类及数目不变,在方程式的空白处应填入:2 H2O;
②由于在制取一瓶NO2时,是固液反应需要加热,所以,用到的仪器有:铁架台、集气瓶、酒精灯 烧瓶等;由于NO2能与水反应,密度比空气大,所以收集时可采用向上排空法;由于NO2能污染空气,必须进行尾气处理;整套实验装置设计组装完毕后必须检查 装置气密性;
③在制取NO2时的生成了硫酸铜溶液和二氧化氮气体,所以实验现象:Ⅰ:溶液由无色变蓝色,Ⅱ:产生红棕色气体;
④反应后的溶液为硫酸铜溶液,可通过蒸发结晶得到硫酸铜晶体.
故答为:(1)高;(2)吸收二氧化硫,避免污染环境、氢氧化钠(或NaOH);(3)节约药品;(4)“下入上出”、间隔;(5)①2 H2O;②集气瓶、酒精灯,向上排空法,装置气密性;③Ⅰ:溶液由无色变蓝色;Ⅱ:产生红棕色气体;④蒸发结晶.
(2)由于二氧化硫是对大气由污染的气体.所以,瓶中预先加水的目的是:吸收二氧化硫,避免污染环境;由于氢氧化钠是一种强碱,能与二氧化硫反应,把水替换为能使酚酞试液的变红色的氢氧化钠溶液;
(3)用点滴板代替试管完成实验的好处是节约药品;
(4)水流经过冷凝管后温度会上升,如果水流方向与气流方向相同,那么在冷凝管末端会出现较热的水在冷却较冷的气体这样的情况.如果反过来的话,同一段冷凝管中的水温和气温差别较大,冷却效果更好.高温水蒸气的冷却,从微观角度看是水分子的间隔 减小了
(5)①根据质量守恒定律反应前后原子的种类及数目不变,在方程式的空白处应填入:2 H2O;
②由于在制取一瓶NO2时,是固液反应需要加热,所以,用到的仪器有:铁架台、集气瓶、酒精灯 烧瓶等;由于NO2能与水反应,密度比空气大,所以收集时可采用向上排空法;由于NO2能污染空气,必须进行尾气处理;整套实验装置设计组装完毕后必须检查 装置气密性;
③在制取NO2时的生成了硫酸铜溶液和二氧化氮气体,所以实验现象:Ⅰ:溶液由无色变蓝色,Ⅱ:产生红棕色气体;
④反应后的溶液为硫酸铜溶液,可通过蒸发结晶得到硫酸铜晶体.
故答为:(1)高;(2)吸收二氧化硫,避免污染环境、氢氧化钠(或NaOH);(3)节约药品;(4)“下入上出”、间隔;(5)①2 H2O;②集气瓶、酒精灯,向上排空法,装置气密性;③Ⅰ:溶液由无色变蓝色;Ⅱ:产生红棕色气体;④蒸发结晶.
点评:本题实验涉及的知识点比较多,但难度不大,应加强实验,提高自己的实验技能.

练习册系列答案
相关题目
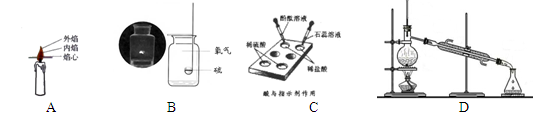 (1)实验A证明蜡烛燃烧产生的火焰,外焰温度最 (填“高”或“低”) 。
(1)实验A证明蜡烛燃烧产生的火焰,外焰温度最 (填“高”或“低”) 。 Cu(NO3)2 +2 NO2↑+ □
Cu(NO3)2 +2 NO2↑+ □ 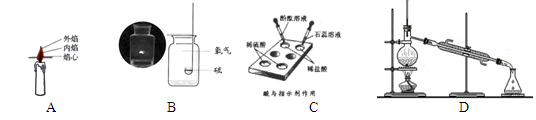 (1)实验A证明蜡烛燃烧产生的火焰,外焰温度最 (填“高”或“低”) 。
(1)实验A证明蜡烛燃烧产生的火焰,外焰温度最 (填“高”或“低”) 。
 Cu(NO3)2+2NO2↑+______;
Cu(NO3)2+2NO2↑+______;