题目内容
计算题(共6分) 相对原子质量:Fe:56 C:12 O:16
我国是世界钢铁产量最大的国家,炼铁的主要原料是铁矿石。用赤铁矿石(主要成分为Fe2O3)炼铁的反应原理为: 3CO+ Fe2O3高温2Fe + 3CO2 。用含Fe2O360%的赤铁矿石800t,理论上可炼出纯铁多少吨?
我国是世界钢铁产量最大的国家,炼铁的主要原料是铁矿石。用赤铁矿石(主要成分为Fe2O3)炼铁的反应原理为: 3CO+ Fe2O3高温2Fe + 3CO2 。用含Fe2O360%的赤铁矿石800t,理论上可炼出纯铁多少吨?
解:设理论上可炼出纯铁的质量为x。
Fe2O3 +3CO高温2Fe + 3CO2
160 112 ………………………………………………………(1分)
800 t×60% x
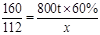 ……………………………………………………………… (1分)
……………………………………………………………… (1分)
x="336" t……………………………………………………………………(1分)
答:理论上可炼出纯铁336 t。
Fe2O3 +3CO高温2Fe + 3CO2
160 112 ………………………………………………………(1分)
800 t×60% x
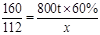 ……………………………………………………………… (1分)
……………………………………………………………… (1分)x="336" t……………………………………………………………………(1分)
答:理论上可炼出纯铁336 t。
本题考查的是含杂质物质的化学反应的有关计算。含杂质物质的化学反应的有关计算是指在实际生产中,所用的原料或产物一般都含有杂质,在利用化学方程式进行计算用料和产量时,由于化学方程式表示的是纯净物质之间的质量关系,而不表示不纯物质之间的质量关系;故计算时一定考虑到杂质的问题,即不纯物质和纯物质之间的相互转化问题。
不纯物质的质量与纯物质的质量的相互转化方法及纯度的计算公式是:
结合赤铁矿石的质量、氧化铁的质量分数,再根据赤铁矿炼铁的化学方程式可以列式计算出理论上可炼出铁的质量。
解:设理论上可炼出纯铁的质量为x。
Fe2O3 +3CO高温2Fe + 3CO2
160 112
800t×60% x
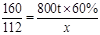
解得x=336t
答:理论上可炼出纯铁336t。
不纯物质的质量与纯物质的质量的相互转化方法及纯度的计算公式是:

结合赤铁矿石的质量、氧化铁的质量分数,再根据赤铁矿炼铁的化学方程式可以列式计算出理论上可炼出铁的质量。
解:设理论上可炼出纯铁的质量为x。
Fe2O3 +3CO高温2Fe + 3CO2
160 112
800t×60% x
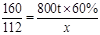
解得x=336t
答:理论上可炼出纯铁336t。

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目