题目内容
如表为元素周期表的部分元素的相关信息,利用表回答相关问题.
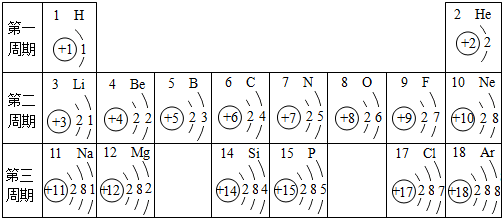
(1)写出13号元索的名称 ,16号元素的原子最外层电子数是 ,17号元素的原子在化学变化中容易 (填“得到”或“失去”)电子.
(2)以上元素中与He化学性质相似的元素有 (写一种).
(3)1、8、11号元素组成碱的俗名是 .
(4)研究表明:第二周期从3-9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小.从而分析第三周期从11-17号元素原子半径变化规律是 .

(1)写出13号元索的名称
(2)以上元素中与He化学性质相似的元素有
(3)1、8、11号元素组成碱的俗名是
(4)研究表明:第二周期从3-9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小.从而分析第三周期从11-17号元素原子半径变化规律是
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:(1)根据核电荷数来确定元素名称,由由原子结构示意图可知13号元素的原子最外层电子数;根据最外层电子数来确定得失电子情况;
(2)He的化学性质稳定,在反应中不容易失去电子也不容易得到电子,则选项中最外层电子数为8的为稳定结构,在反应中不容易失去也不容易得到电子,即与He具有相似化学性质.
(3)确定元素名称,再书写化学式;
(4)根据元素周期表的变化规律进行解答.
(2)He的化学性质稳定,在反应中不容易失去电子也不容易得到电子,则选项中最外层电子数为8的为稳定结构,在反应中不容易失去也不容易得到电子,即与He具有相似化学性质.
(3)确定元素名称,再书写化学式;
(4)根据元素周期表的变化规律进行解答.
解答:解:(1)13号元素是铝元素,16号元素最外层应该有6个电子,17号元素最外层有7个电子,在化学反应中易得到1个电子;故填:铝;6;得到;
(2)He的化学性质稳定,在反应中不容易失去电子也不容易得到电子,氖和氩最外层是8个电子,极不易得到电子,也不易失去电子,故与氦元素化学性质相似;故填:Ne或Ar;
(3)1号元素是氢元素,8号元素是氧元素,11号元素是钠元素,组成的碱是氢氧化钠,俗称火碱、烧碱、苛性钠;故填:火碱或烧碱或苛性钠;
(4)根据元素周期表的变化规律可知:第二周期从3号--9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小.我分析第三周期从11号--17号元素原子半径变化规律是随核电荷数增大,原子半径逐渐减小;故填:随核电荷数增大,原子半径逐渐减小.
(2)He的化学性质稳定,在反应中不容易失去电子也不容易得到电子,氖和氩最外层是8个电子,极不易得到电子,也不易失去电子,故与氦元素化学性质相似;故填:Ne或Ar;
(3)1号元素是氢元素,8号元素是氧元素,11号元素是钠元素,组成的碱是氢氧化钠,俗称火碱、烧碱、苛性钠;故填:火碱或烧碱或苛性钠;
(4)根据元素周期表的变化规律可知:第二周期从3号--9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小.我分析第三周期从11号--17号元素原子半径变化规律是随核电荷数增大,原子半径逐渐减小;故填:随核电荷数增大,原子半径逐渐减小.
点评:本题考查学生根据原子结构示意图分析总结元素周期律及对元素的性质与最外层电子数的关系的理解与掌握,并能在解题中灵活应用.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
下列做法正确的是( )
| A、加入适量的氢氧化钡溶液以除去NaCl溶液中的少量Na2SO4 |
| B、加入适量的碳酸钙粉末以除去盐酸溶液中的少量CaCl2 |
| C、用氢氧化钠溶液处理硫在氧气中燃烧产生的气体 |
| D、用点燃的方法除去CO2中混有的少量CO |