题目内容
我市有丰富的NaCl矿产资源,NaCl是一种重要的化工原料,可以用于生产烧碱、氯气等重要的化工产品。某化工厂购进一批以NaCl为主要成分的原料(假设杂质全部为CaCl2),化验员欲测定原料中NaCl的质量分数,先称取60.0g样品,加足量水充分溶解后,向所得溶液中加入足量的溶质质量分数为10%的Na2CO3溶液,充分反应后,生成2.0g白色沉淀。(已知:CaCl2+Na2CO3==2NaCl+CaCO3↓)
试回答下列问题(写出计算过程):
(1)原料中NaCl的质量分数是多少?
(2)当恰好完全反应时,需Na2CO3溶液的质量是多少?
试回答下列问题(写出计算过程):
(1)原料中NaCl的质量分数是多少?
(2)当恰好完全反应时,需Na2CO3溶液的质量是多少?
解:设原料中CaCl2的质量为X,当恰好完全反应时,需Na2CO3溶液的质量为Y
CaCl2+Na2CO3==2NaCl+CaCO3↓
111 106 100
X Y×10% 2.0g
(1)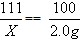 X=2.22g
X=2.22g
原料中NaCl的质量分数=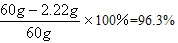
(2)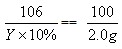
Y=21.2g
CaCl2+Na2CO3==2NaCl+CaCO3↓
111 106 100
X Y×10% 2.0g
(1)
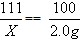 X=2.22g
X=2.22g原料中NaCl的质量分数=
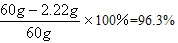
(2)
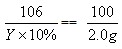
Y=21.2g

练习册系列答案
相关题目
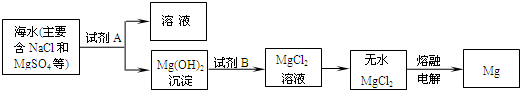
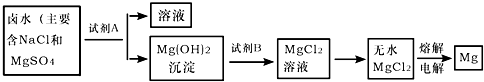
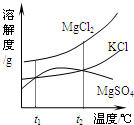 我市濒临渤海,有较长的海岸线,海洋资源十分丰富.
我市濒临渤海,有较长的海岸线,海洋资源十分丰富.