��Ŀ����
��9�֣�ij����С����ѧϰ��ͭ��������Ӧ(2Cu+O2��2CuO)��һ���ʺ�����һ�������������������IJⶨ��ʵ�飬�������ͭ˿���л��ա�
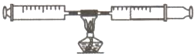
(1)����С��Կ��������������IJⶨ��������ʵ�飺��������ע������ɵ��ܱ�ϵͳ����50 mL��������ͼ��Ȼ���װ��ͭ˿�IJ����ܼ��ȡ�ͬʱ�����ƶ�����ע�����Ļ��������������ڵ�ͭ˿����ҽϳ�ʱ������һ���仯ʱֹͣ��ֹͣ���Ⱥ���ȴ�����½�����ȫ������һ��ע�����ڡ�
������������ʵ������⣬�ش��������⣺
��ʵ�������ע�����ڿ��������������Լ mL��������Ϊ
����ʵ��ļ��ȹ����У����滺���ƶ�����ע������Ŀ���� ��
������ʵ��ֻ�Ǵ��Բⶨ����������������һ�ַ���������Ϊ��ɸ�ʵ�鲻����ȷ��
����ԭ���� ��
(2)����С�鷢�ֺ��ȵ�ͭ˿��ں�Ϊ�˻���������ͭ˿�����о���γ�ȥ��ɫ
���ʵ������У��ƶ������з�����
��������Ϸ����ش�
�� �ҷ������ձ��з�����Ӧ�Ļ�ѧ����ʽΪ
���ַ�����Ƚϣ������IJ���֮���� ��
�������üס������ַ��������˱�ɺ�ɫ��ͭ˿�����ҳ�ַ�Ӧ������յ�ͭ˿a����
�� (�<������>������=��)ͭ˿b��������
��9�֣���1�� �� 10 �������������Լռ 1/5 . ����1�֣��� ��ͭ�����������Ӧ����1�֣���ͭ˿δ����ȫ���ĵ�ע�����ڵ�������װ��©������2�֣�
��2���� CuO + 2HCl == CuCl2 + H2O;��1�֣� CO�ж���β��COδ������ʵ��װ�ø��ӵȡ���2�֣��� > ��1�֣�
����:��

 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�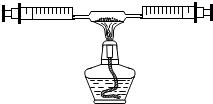 ij����С����ѧϰ���鱾�����������������IJⶨ��ʵ�飬֪��P2O5��������ŷ��ڿ����У������Կ��������Ⱦ�����ԶԸ�ʵ������˸Ľ���
ij����С����ѧϰ���鱾�����������������IJⶨ��ʵ�飬֪��P2O5��������ŷ��ڿ����У������Կ��������Ⱦ�����ԶԸ�ʵ������˸Ľ���
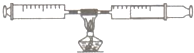 ij����С����ѧϰ���鱾�����������������IJⶨ��ʵ�飬֪�����������ײ�������ŷ��ڿ����У������Կ��������Ⱦ�����ԶԸ�ʵ������˸Ľ���
ij����С����ѧϰ���鱾�����������������IJⶨ��ʵ�飬֪�����������ײ�������ŷ��ڿ����У������Կ��������Ⱦ�����ԶԸ�ʵ������˸Ľ���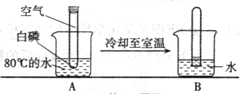 ij����С����ѧϰ���鱾�����������������IJⶨ��ʵ�飬֪��P2O5��������ŷ��ڿ����У������Կ��������Ⱦ�����ԶԸ�ʵ������˸Ľ�������ͼ��ʾ��
ij����С����ѧϰ���鱾�����������������IJⶨ��ʵ�飬֪��P2O5��������ŷ��ڿ����У������Կ��������Ⱦ�����ԶԸ�ʵ������˸Ľ�������ͼ��ʾ�� ��1����ͼ��С��ͬѧ�ӵ�ȼ���������������һ�ơ����̡���ʵ��װ�ã�С��ͬѧ��Ϊ�����̡��ijɷ���ˮ������С��ͬѧ��Ϊ�����̡��ijɷ��������������������̽����ȷ�������̡��ɷ֣���֤С��ͬѧ�������õķ�����
��1����ͼ��С��ͬѧ�ӵ�ȼ���������������һ�ơ����̡���ʵ��װ�ã�С��ͬѧ��Ϊ�����̡��ijɷ���ˮ������С��ͬѧ��Ϊ�����̡��ijɷ��������������������̽����ȷ�������̡��ɷ֣���֤С��ͬѧ�������õķ�����