题目内容
某同学欲除去氯化钠固体中混有的氯化钙,设计了如下方案,请完成实验报告.
(1)溶解:将混合物放入烧杯里,加入足量水,用玻璃棒搅拌,使其充分溶解,得到无色溶液,玻璃棒搅拌的目的是 .
(2)过滤:向上述溶液中加入碳酸钠溶液,使其充分反应,产生白色沉淀,过滤后取液,滤液呈无色,加入过量碳酸钠溶液的目的是除去 ,反应的化学方程式是 .
(3)蒸发:向上述滤液中逐滴加入稀盐酸,直到不产生气泡为止,将溶液倒入蒸发皿中蒸发,直到析出晶体.滴加稀盐酸的目的是除去多余的 .
(1)溶解:将混合物放入烧杯里,加入足量水,用玻璃棒搅拌,使其充分溶解,得到无色溶液,玻璃棒搅拌的目的是
(2)过滤:向上述溶液中加入碳酸钠溶液,使其充分反应,产生白色沉淀,过滤后取液,滤液呈无色,加入过量碳酸钠溶液的目的是除去
(3)蒸发:向上述滤液中逐滴加入稀盐酸,直到不产生气泡为止,将溶液倒入蒸发皿中蒸发,直到析出晶体.滴加稀盐酸的目的是除去多余的
考点:物质除杂或净化的探究,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的分离、除杂、提纯与共存问题
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:(1)欲除去氯化钠固体中混有的氯化钙,将混合物放入烧杯里,加入足量水,用玻璃棒搅拌,使其充分溶解,得到无色溶液,玻璃棒搅拌的目的是加快混合物的溶解速率.
(2)向上述溶液中加入碳酸钠溶液,碳酸钠能与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,使其充分反应,产生白色沉淀,过滤后取液,滤液呈无色,加入过量碳酸钠溶液的目的是除去溶液中的氯化钙;反应的化学方程式为:CaCl2+Na2CO3═CaCO3↓+2NaCl.
(3)过滤后,滤液中含有氯化钠、碳酸钠(过量的),向上述滤液中逐滴加入稀盐酸,碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,滴加稀盐酸的目的是除去多余的碳酸钠溶液,直到不产生气泡为止,将溶液倒入蒸发皿中蒸发,直到析出晶体.
故答案为:(1)加快混合物的溶解速率;(2)溶液中的氯化钙;CaCl2+Na2CO3═CaCO3↓+2NaCl;(3)碳酸钠溶液.
(2)向上述溶液中加入碳酸钠溶液,碳酸钠能与氯化钙溶液反应生成碳酸钙沉淀和氯化钠,使其充分反应,产生白色沉淀,过滤后取液,滤液呈无色,加入过量碳酸钠溶液的目的是除去溶液中的氯化钙;反应的化学方程式为:CaCl2+Na2CO3═CaCO3↓+2NaCl.
(3)过滤后,滤液中含有氯化钠、碳酸钠(过量的),向上述滤液中逐滴加入稀盐酸,碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,滴加稀盐酸的目的是除去多余的碳酸钠溶液,直到不产生气泡为止,将溶液倒入蒸发皿中蒸发,直到析出晶体.
故答案为:(1)加快混合物的溶解速率;(2)溶液中的氯化钙;CaCl2+Na2CO3═CaCO3↓+2NaCl;(3)碳酸钠溶液.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
下列化学方程式符合题意且书写正确的是( )
| A、用红磷测定空气中氧气的含量4P+5O2═4P2O5 | ||||
B、用高锰酸钾制氧气2KMnO4
| ||||
| C、检验二氧化碳气体CO2+2NaOH═Na2CO3+H2O | ||||
D、铁丝在氧气中燃烧:3Fe+2O2
|
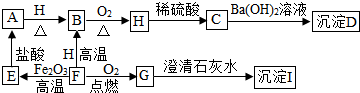
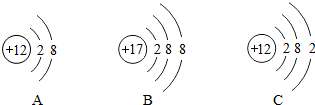
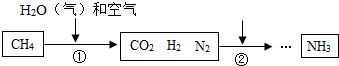
 锂是手机电源的重要材料,如图是锂原子的构成示意图,根据图示信息回答下列问题:
锂是手机电源的重要材料,如图是锂原子的构成示意图,根据图示信息回答下列问题: