题目内容
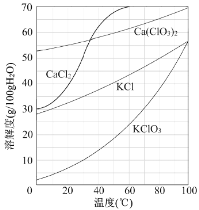
【题目】甲、乙两种固体物质的溶解度曲线如右图所示。下列说法不正确的是
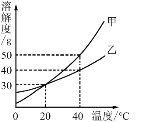
A. 40℃时,甲的溶解度大于乙的溶解度
B. 从甲溶液中提取甲物质适合用冷却热饱和溶液结晶
C. 20℃时,甲乙溶液中溶质的质量分数一定相等
D. 将40℃时乙的饱和溶液降温至20℃,仍然是饱和溶液
【答案】C
【解析】
A、通过分析溶解度曲线可知,40℃时,甲的溶解度大于乙的溶解度,故A正确;
B、甲物质的溶解度受温度变化影响较大,所以从甲溶液中提取甲物质适合用冷却热饱和溶液结晶,故B正确;
C、20℃时,甲、乙物质的溶解度相等,所以饱和溶液中溶质的质量分数一定相等,题中未指明溶液是否饱和,故不能判断甲乙溶液质量分数大小,故C错误;
D、乙物质的溶解度随温度降低而减小,所以将40℃时乙的饱和溶液降温至20℃,仍然是饱和溶液,故D正确。故选C。

练习册系列答案
相关题目
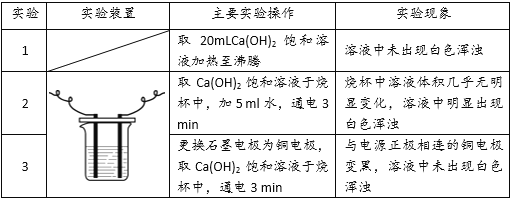
【题目】分类、类比推理都是学习化学常用的方法。
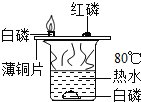
(1)在A、B、C、D实验中,某些实验设计的原理是相同的。
稀释浓硫酸 | 探究燃烧条件 | 探究中和反应 | 探究铁钉生锈 |
|
|
|
|
A | B | C | D |
其中实验B与_____(填字母)归为一类,依据是它们都采用____________的科学方法。
(2)过量的CO2能与Ca(OH)2反应如下: Ca(OH)2+2CO2==Ca(HCO3)2;

同理过量的CO2也能与NaOH反应:NaOH+CO2==NaHCO3
写出侯德榜(如图纪念邮票)制碱法的第一步反应:向氨水中通入过量的CO2反应的化学方程式为_____________________;在第二步利用减压蒸发方法获取副产品NH4Cl,在当时,它的用途是用作_________,这也是侯德榜对人类的贡献之一。