题目内容
【题目】现有20g纯碱样品(含有少量氯化钠),放入烧杯中加入100g稀盐酸后恰好完全反应,反应后烧杯中溶液总质量为113.4g。试计算:
(1)反应生成二氧化碳的质量是______g;
(2)纯碱样品中纯碱的质量分数_____。(提示:Na2CO3+2HCl==2NaCl+H2O+CO2↑)
【答案】6.6 79.5%
【解析】
根据化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑,可知反应前后减少的质量就是生成二氧化碳的质量,
(1)根据化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑,由质量守恒定律可知反应前后减少的质量就是生成二氧化碳的质量,是20g+100g-113.4g=6.6g
(2)设样品中碳酸钠的质量为x
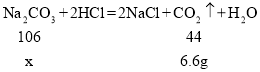
![]()
![]()
样品中碳酸钠的质量分数:
![]()

练习册系列答案
相关题目