题目内容
张化验员对本炼铁厂购进的赤铁矿(主要成分三氧化二铁)样品进行分析.取10g的样品,完全反应后,共用去稀盐酸100g,过滤后得到2g滤渣 (假设杂质既不溶于酸,也不溶于水;不考虑实验中的损耗).
求(结果精确到1%):
(1)赤铁矿样品中Fe2O3的质量分数为多少?
(2)稀盐酸中溶质的质量分数为多少?
求(结果精确到1%):
(1)赤铁矿样品中Fe2O3的质量分数为多少?
(2)稀盐酸中溶质的质量分数为多少?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)滤渣质量就是样品中杂质的质量,由杂质质量和样品质量可以计算出样品中氧化铁的质量.
(2)由氧化铁的质量根据氧化铁与稀盐酸反应的化学方程式可以计算出稀盐酸中溶质的质量分数.
(2)由氧化铁的质量根据氧化铁与稀盐酸反应的化学方程式可以计算出稀盐酸中溶质的质量分数.
解答:解:(1)样品中氧化铁的质量为:10g-2g=8g
(2)设稀盐酸中溶质的质量分数为x.
Fe2O3+6HCl=2FeCl3+3H2O
160 219
8g 100g×x
=
,
x=10.95%
答:赤铁矿石样品中Fe2O3的质量为8g,稀盐酸中溶质的质量分数为10.95%.
(2)设稀盐酸中溶质的质量分数为x.
Fe2O3+6HCl=2FeCl3+3H2O
160 219
8g 100g×x
| 160 |
| 8g |
| 219 |
| 100g×x |
x=10.95%
答:赤铁矿石样品中Fe2O3的质量为8g,稀盐酸中溶质的质量分数为10.95%.
点评:本题主要考查含杂质物质的化学方程式计算,难度稍大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
下列图示实验操作中正确的是( )
A、 |
B、 |
C、 |
D、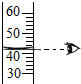 |
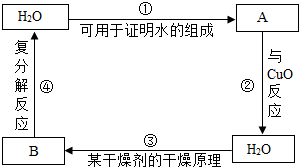 课外活动时,同学们玩起了在特定条件下,以水为主题的“化学反应接龙”(前一反应的一种生成物为下一反应的反应物)游戏,请按要求回答问题.
课外活动时,同学们玩起了在特定条件下,以水为主题的“化学反应接龙”(前一反应的一种生成物为下一反应的反应物)游戏,请按要求回答问题.
 随着生活质量的提高,人们越来越关注自身的健康.
随着生活质量的提高,人们越来越关注自身的健康. 如图为A、B、C三种固体物质的溶解度曲线,据图回答:
如图为A、B、C三种固体物质的溶解度曲线,据图回答: