题目内容
【题目】兴趣小组对“一氧化碳还原氧化铜”的实验进行改进。
(查阅资料及准备)
Ⅰ. 甲酸在 98%硫酸溶液催化下的反应为:HCOOH ![]() H2O+CO 。
H2O+CO 。
Ⅱ. 一氧化碳的爆炸极限(混合气体中的体积分数)为:12.5%-75%。
Ⅲ. 经测量,下图装置中试管、干燥管和 D 处前导管的总体积为 80mL。在广口瓶的适当位置绘制放置爆炸的安全线。
(设计方案)实验装置如下(固定装置略):
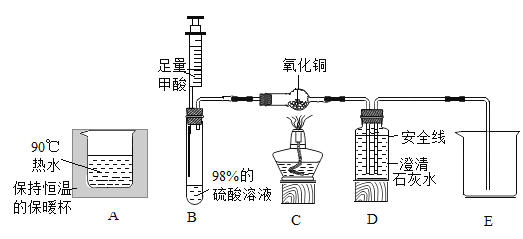
实验步骤 | 现象 | 分析和结论 |
Ⅰ. 检查气密性。按上图连接装置,D 处瓶中装满水,推动空注射器 | D 处导管口产生气泡 | 说明整套装置_____(选填“漏气”或“不漏气”) |
Ⅱ. 装入药品,进行反应。把 B 装置放入A 中,逐滴滴入甲酸,待 D 处液面下降至安全线处,点燃酒精灯。反应完成后,熄灭酒精灯。装置冷却后取出 B | C 处黑色粉末变为红色 | C 处反应的化学方程式为_____ |
Ⅲ. 尾气处理,打开D 处瓶塞,点燃瓶内气体 | 瓶口出现蓝色火焰 | 尾气处理的目的是_____ |
(实验分析)
(1)待 D 处液面下降至安全线处,再点燃酒精灯是为了_____。
(2)能证明 CuO 已知 CO 发生反应的现象有_____。
(3)若 B 处有a mol 甲酸参加反应,D 处生成 b mol 碳酸钙,则a>b,理由是_____。
(4)假设装置内空气已全部排入D 处瓶中,当瓶内气体体积为 400mL 时,点燃是否发生爆炸? 通过计算说明理由(不考虑药品的体积)_____。
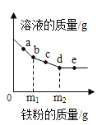
(5)逐滴滴入甲酸后,符合如图变量 y 的是_____
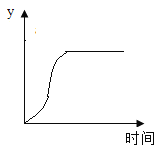
a、B 处水的物质的量
b、B 处生成一氧化碳的质量
c、C 处生成金属铜的物质的量
d、D 处碳酸钙的质量
【答案】不漏气 CO+CuO![]() Cu+CO2 防止CO排出污染环境 防止CO与空气混合加热发生爆炸 C中黑色固体变红 部分CO未参与反应 不爆炸;CO的体积分数为80%,不在爆炸极限范围内 b
Cu+CO2 防止CO排出污染环境 防止CO与空气混合加热发生爆炸 C中黑色固体变红 部分CO未参与反应 不爆炸;CO的体积分数为80%,不在爆炸极限范围内 b
【解析】
本题是对“一氧化碳还原氧化铜”的实验改进与设计,要根据资料和实验设计方案分析解答。
检查装置气密性,推动空注射器使装置内压强增大,D 处导管口产生气泡,说明装置气密性良好,选填不漏气。
C 处是生成的一氧化碳气体与氧化铜反应,化学方程式为CO+CuO![]() Cu+CO2。
Cu+CO2。
点燃D收集的气体,防止有毒的CO排出污染环境。
(1)待 D 处液面下降至安全线处,再点燃酒精灯是为了装置内收集的一氧化碳气体超出爆炸极限,防止CO与空气混合加热发生爆炸。
(2)CuO 与CO 发生反应,生成铜和二氧化碳,现象是黑色粉末会变红色。
(3)若 B 处有a mol 甲酸参加反应,D 处生成 b mol 碳酸钙,根据质量守恒定律和方程式计算,a=b;如果a>b,理由是部分CO未参与反应。
(4)根据题目可知装置内气体体积为80mL,且全部排入D 处瓶中,那么D 处瓶中空气体积分数为![]() ,D 处瓶中一氧化碳的体积分数为
,D 处瓶中一氧化碳的体积分数为![]() ,超出一氧化碳的爆炸极限,所以不爆炸。
,超出一氧化碳的爆炸极限,所以不爆炸。
(5)
a、在反应前B 处已经有水,所以曲线起点不应该从零点起,不符合题意;
b、反应一开始B 处就产生一氧化碳,符合题意;
c、B 处产生一氧化碳才能与C 处氧化铜反应生成金属铜,曲线起点从零点起错误,不符合题意;
d、D 处碳酸钙的质量,曲线起点从零点起错误,不符合题意。故选b。