题目内容
【题目】在实验室,同学们用如图所示装置研究了水的组成。请回答以下问题。
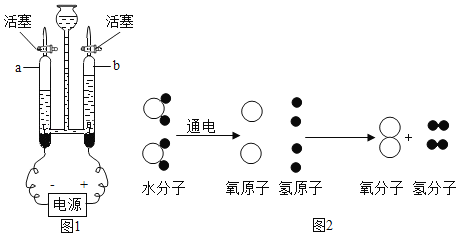
(1)实验一段时间后,切断电源,用燃着的木条分别放在a、b两个玻璃管尖嘴口,打开活塞,观察到的现象是____________,实验可得出有关水的组成的结论是_____。
(2)如图是电解水的微观过程示意图,请你从微观视角分析电解水遵守质量守恒定律的原因______________________________。
【答案】b处木条燃烧更剧烈、a处气体燃烧,发出淡蓝色火焰 水由氢元素和氧元素组成 反应前后原子种类、总个数和质量都不变
【解析】
根据水电解实验的现象、产物的检验、结论进行分析。
(1)用燃着的木条分别放在a、b两个玻璃管尖嘴口,打开活塞,观察到的现象是:b处木条燃烧更剧烈、a处气体燃烧,发出淡蓝色火焰,说明生成的气体分别是氧气、氢气,进一步说明水是由氢元素和氧元素组成的。
故填:b处木条燃烧更剧烈、a处气体燃烧,发出淡蓝色火焰;水由氢元素和氧元素组成。
(2)从微观视角分析电解水遵守质量守恒定律的原因是反应前后原子种类、总个数和质量都不变。
故填:反应前后原子种类、总个数和质量都不变。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】早在十七世纪,英国化学家波义耳由于实验设计“失误”,错过了发现质量守恒定律的机会,请你改进他的试验方法,以验证质量守恒定律。
波义耳的实验(1673年) | 我的改进 |
在密闭的容器中燃烧金属,得到了金属灰 | 称量密闭的容器(连同里面的金属),进行燃烧实验 |
打开容器,称量金属灰的质量 | 燃烧结束后,称量________________ |
发现比原金属质量_____________(填“增加”或“减少”或“不变”) | 发现总质量和燃烧前一样。若反应容器内的反应是镁带燃烧,其反应的化学方程式是 _____________________________________ |
启发:用实验来研究化学反应前后反应物和生成物之间的质量关系时,应该在______________ 容器中进行。 | |
拓展:应用质量守恒定律验证石墨的元素组成。 实验步骤:称量a克石墨,放在盛有足量氧气的密闭容器中引燃;反应结束后,用足量的b克澄清石灰水吸收生成的气体(吸收完全),发生的反应方程式为:____________________ 称量石灰水的质量变为c克。 根据______________________________(现象),可知石墨中含有碳元素; 根据a=_______________________(用含b、c的关系式表示),可知石墨中只含有碳元素 | |
【题目】某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。
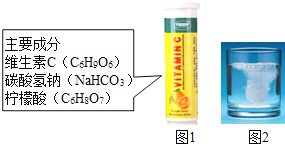
探究一:该气体的成分。
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为_________________________。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO_____________________________。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
实验编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
【得出结论】(1)由实验①可知,该气体中肯定含有_________,写出该反应的化学方程式________________。
(2)由实验②____________(填“能”或“不能”)确定该气体中不含氧气,理由是______________________。
探究二:维C泡腾片溶液的酸碱性。
向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显_________性。