题目内容
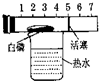 活塞左端管内密封有空气,右端的管口跟空气连通.将玻璃容器固定在盛有
活塞左端管内密封有空气,右端的管口跟空气连通.将玻璃容器固定在盛有80℃热水(恒温)的烧杯上,进行测定空气中氧气含量的实验.请回答下列问题:
(1)整个实验过程中观察到的现象是
(2)请用理化知识解释冷却至室温后所产生现象的原因
考点:空气组成的测定
专题:空气与水
分析:将玻璃容器固定在盛有80℃热水(恒温)的烧杯上,产生大量的白烟,放出大量的热;白磷燃烧与氧气反应生成五氧化二磷固体,使管内气体减少,装置内压强减小,在压强差的作用活塞向左移动,据此结合空气中氧气的含量判断出现的现象.
解答:解:(1)白磷燃烧,产生大量的白烟,放出大量的热,装置内的气体受热体积会膨胀,所以活塞向右滑动;反应结束后,随着温度的降低,最终完全恢复至室温后,气体的体积慢慢收缩,活塞向左滑动.由于氧气被消耗掉,氧气约占空气体积的
,故装置冷却后活塞左移
,到达处4刻度处,活塞最终停在刻度“4”处;
(2)白磷燃烧,与氧气反应生成五氧化二磷,消耗氧气,生成五氧化二磷固体,使管内气体减少,装置内压强减小,小于外界压强,在压强差的作用,活塞向左移动,由于氧气约占空气体积的五分之一,所以活塞停留在4格处.
故答案为:(1)白磷燃烧,产生大量的白烟,活塞先向右移动,冷却后再向左移动,最终停留在4格处.
(2)白磷燃烧与氧气反应生成五氧化二磷固体,使管内气体减少,装置内压强减小,在压强差的作用,活塞向左移动,由于氧气约占空气体积的五分之一,所以活塞停留在4格处.
| 1 |
| 5 |
| 1 |
| 5 |
(2)白磷燃烧,与氧气反应生成五氧化二磷,消耗氧气,生成五氧化二磷固体,使管内气体减少,装置内压强减小,小于外界压强,在压强差的作用,活塞向左移动,由于氧气约占空气体积的五分之一,所以活塞停留在4格处.
故答案为:(1)白磷燃烧,产生大量的白烟,活塞先向右移动,冷却后再向左移动,最终停留在4格处.
(2)白磷燃烧与氧气反应生成五氧化二磷固体,使管内气体减少,装置内压强减小,在压强差的作用,活塞向左移动,由于氧气约占空气体积的五分之一,所以活塞停留在4格处.
点评:本题难度不大,掌握测定空气中氧气含量的实验原理、白磷燃烧的现象等是正确解答本题的关键.

练习册系列答案
相关题目
下列反应属于分解反应的是( )
| A、蜡烛+氧气═二氧化碳+水 |
| B、水═氢气+氧气 |
| C、氢气+氧气═水 |
| D、锌+盐酸═氯化锌+氢气 |
下列常见的现象,属于化学变化的是( )
| A、硝酸铵溶于水 |
| B、浓盐酸敞放 |
| C、生石灰溶于水 |
| D、浓硫酸敞放 |
 在今天的化学兴趣小组活动中,指导老师拿来了一包白色固体.老师告诉同学们说,这包白色固体可能是由Ca(OH)2和CaCO3中的一种或两种组成.为了确定该白色固体的组成,同学们进行了如下的探究活动:
在今天的化学兴趣小组活动中,指导老师拿来了一包白色固体.老师告诉同学们说,这包白色固体可能是由Ca(OH)2和CaCO3中的一种或两种组成.为了确定该白色固体的组成,同学们进行了如下的探究活动: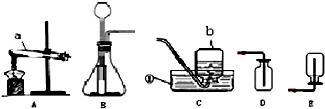

 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题: