��Ŀ����
����Ŀ�����÷�����ͭ��Cu��Ni������õ�Cu��Ni���ֽ���������Ҫ�������£�
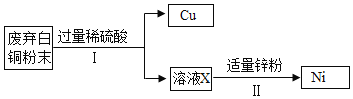
��֪��Ni��Fe��ѧ�������ƣ��������ϼ�Ϊ+2�ۡ�
��1��������з�Ӧ�Ļ�ѧ����ʽΪ_________��
��2��������з�Ӧ���ڻ�����Ӧ�����е�_______��
���𰸡�Ni+H2SO4=NiSO4+H2�� �û���Ӧ
��������
��1���������ͭ�Dz����ý���������ϡ���ᷴӦ��Ni����Fe��ѧ�������ƣ���ϡ���ᷴӦ����NiSO4����������Ӧ�Ļ�ѧ����ʽΪNi+H2SO4=NiSO4+H2�������Ni+H2SO4=NiSO4+H2����
��2������1��������֪����ҺX�����ʾ�����������������м�������п����п�����������е����û�������ͬʱ��������п���÷�Ӧ����һ�ֵ�����һ�ֻ����ﷴӦ��������һ�ֵ��ʺ���һ�ֻ���������ķ�Ӧ�����û���Ӧ������û���Ӧ��

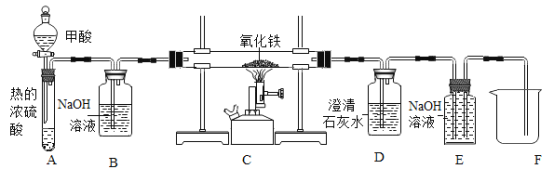
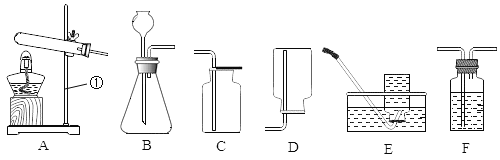
����Ŀ����������ͼ��ʾ�������ʵ�飬���������ﵽʵ��Ŀ�ĵ��ǣ�������
ʵ��Ŀ�� | ʵ�鲽�� | |
A | �Ƚ�����ͭ�Ľ������ǿ�� | �ټ���ͭ��ĩ���ڼ�������ϡ������裻�ۼ�����Ƭ |
B | ����NaCl�л���Na2CO3 | �ټ���������Ʒ���ڼ�������ˮ��ȫ���ܽ⣻ �ۼ�������ϡ���� |
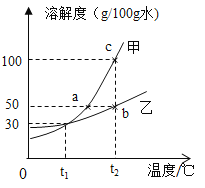
C | ��֤KCl���������ܽ� | 20��Cʱ���ټ���100gˮ���ڼ���18gKCl���裻�ۼ���16gKCl���裨��֪��20��ʱ��KCl���ܽ��Ϊ34g�� |
D | ����50g������������Ϊ5%���Ȼ�����Һ | �ټ���2.5gNaCl���ڼ���47.5gˮ���۽�����ȫ���ܽ� |
A.AB.BC.CD.D