题目内容
【题目】下列说法不正确的是( )
A. 由Na![]() 和K
和K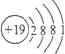 得出,钠元素和钾元素的化学性质相似
得出,钠元素和钾元素的化学性质相似
B. 石墨在高温高压催化剂作用下转化为金刚石,这是物理变化
C. CO会与血液中的血红蛋白结合导致中毒
D. 金刚石与石墨物理性质存在很大的差异,是因为构成它们的碳原子排列方式不同
【答案】B
【解析】A、元素原子的化学性质是由最外层电子数决定的,因此最外层电子数相同的微粒具有相似的化学性质,故选项正确;
B、石墨和金刚石属于不同物质,所以石墨在高温高压催化剂作用下转化为金刚石,这是化学变化,故选项错误;
C、CO具有毒性,一氧化碳与血液中的血红蛋白结合导致中毒,故选项正确;
D、金刚石、石墨碳的单质物理性质存在很大的差异,是因为构成它们的碳原子排列方式不同,故选项正确。

【题目】“酸、碱和盐的溶解性表(室温)”是学习化学的重要工具,智慧小组同学利用该工具进行探究学习。
探究活动一:认识工具
如下图,表中标注了甲、乙、丙、丁和戊五种物质,物质的溶解性均未标明。
部分酸、碱和盐的溶解性表(室温)
阴离子 阳离子 | OH- | NO3- | Cl- | SO42- | CO32- |
| 乙 | 丙 | |||
| 甲 | 丁 | 戊 |
(1)认识符号:NO3-名称是________;
(2)写化学式:丙物质的化学式是________;
(3)物质分类:五种物质中,属于碱的是________(用化学式表示);
(4)溶解能力:五种物质中,只有一种不溶于水,它是________(用化学式表示)。
探究活动二:运用工具
有一包白色粉末可能含有氯化钡、碳酸钡、碳酸钠、氢氧化钠和硫酸钠中的一种或几种,取一定量该粉末样品加入到盛有足量水的烧杯中,搅拌,静置,观察到烧杯中有白色不溶物,小郑同学将烧杯中的物质过滤,得滤渣A和滤液B,取滤渣A于试管中滴加过量稀硝酸,观察到滤渣全部溶解,有气泡产生。
小杨同学进一步设计了如下实验方案,确定白色粉末的组成:

针对上述实验方案中各步骤的现象,小杨同学提出下列三种不同的假设,依据每种假设中各步骤不同的实验现象,可得出不同的实验结论。
步骤一 | 步骤二 | 步骤三 | |
假设一 | 有白色沉淀生成 | ||
无白色沉淀生成 | 溶液变红 | 溶液变为无色 | |
假设三 | 无白色沉淀生成 | 无明显现象 | 无明显现象 |
(1)依据假设一的现象,可确定原白色粉末中只含有碳酸钡、碳酸钠、氢氧化钠和硫酸钠四种物质。则步骤二的现象是________;步骤三中发生的任意一个化学反应的化学方程式是________。
(2)依据假设二的现象,原白色粉末可能的组成是________。(任写一种可能的组成,用化学式表示);
(3)依据假设三的现象,原白色粉末可能的组成有________种。
【题目】焙制糕点所用的发酵粉的主要成分之一是碳酸氢钠。某化学兴趣小组对碳酸氢钠的化学性质进行探究:
(探究实验一)实验室里,可用_____测定碳酸氢钠溶液的酸碱度。若测得碳酸氢钠溶液的pH为10,由此得出的结论是碳酸氢钠溶液显_____。
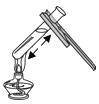
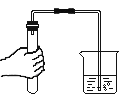
(探究实验二)碳酸氢钠的热稳定性:取一定量的碳酸氢钠放在铜片上加热,如图所示。

(查阅资料)碳酸氢钠受热易分解,生成水、二氧化碳气体和一种常见的固体物质。
(1)加热一段时间后观察烧杯内壁有水珠.
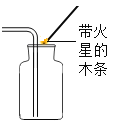
(2)充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,振荡,观察到_____;
(3)该兴趣小组的同学认为充分加热后的固体产物可能是NaOH或Na2CO3。
①他们猜想的依据是_____;
②请设计实验,检验反应后的固体产物是NaOH或Na2CO3,并完成如表:
限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管
序号 | 实验操作 | 预期现象 | 结论 |
Ⅰ | 取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,加入足量_____,振荡,静止 | 产生白色沉淀 | 产物含Na2CO3 |
Ⅱ | 取Ⅰ操作后的上层清液于试管B中,滴加酚酞溶液 | _____ | 产物不含NaOH |