题目内容
【题目】质量守恒定律是自然界的普遍规律,它的发现对化学的发展做出了重要贡献。
(1)下列各组试剂中,通过称量在密闭容器内混合前后的总质量,不能验证质量守恒定律的是____(填字母)。
A.碘和酒精 B.碳酸钠粉末和少量稀盐酸
C.铁和氯化铜溶液 D.氢氧化钠溶液和硫酸铜溶液
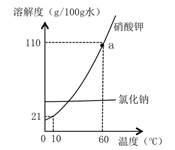
(2)1774年,拉瓦锡用精确的定量实验研究了汞和氧气反应的质量关系。若用一定质量的汞和足量氧气充分反应,生成固体的情况如图所示,则有关反应的化学方程式为__________;参加反应的氧气质量为__________g。

(3)如图是某反应的微观示意图。
![]()
①该反应类型______(填“属于”或“不属于”)置换反应;其中化合价发生改变的元素是_____。
②已知:Cl2+2NaOH=NaCl+NaClO+H2O。氯气和熟石灰反应可以制得漂白粉,该反应的化学方程式为____________;Ca(ClO)2在空气中与二氧化碳和水反应会转化为CaCO3和HClO,该反应的化学方程式为____________。
(4)实验室取34g过氧化氢溶液和1g二氧化锰混合制取氧气,充分反应后,称量剩余溶液和滤渣为34. 2g。则所取过氧化氢溶液中溶质的质量分数是多少?______
【答案】 A 2Hg+O2![]() 2HgO 1.6g 不属于 Cl 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO 5%
2HgO 1.6g 不属于 Cl 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO 5%
【解析】(1). 质量守恒定律是参加反应的各物质的质量总和等于生成的各物质的质量总和;碘和酒精是溶解作用形成溶液,是物理变化,不能用于验证质量守恒定律; (2). 汞和足量氧气充分反应生成氧化汞,反应方程式为:2Hg+O2加热2HgO (3).由图可知,生成氧化汞的质量为21.7g,设参加反应的氧气的质量为x,
2Hg + O2加热 2HgO
32 434
x 21.7g
32/x=434/21.7g x=1.6g
(4). 由一中单质和一种化合物生成另一种和另一种化合物的反应叫置换反应。 (5). 单质中元素的化合价为零,化合物中元素的化合价的代数和为零, 因此可知氯元素反应前后化合价发生改变; (6). Cl2+2NaOH=NaCl+NaClO+H2O。熟石灰和盐酸生成氯化钙,和次氯酸生成次氯酸钙,氯气和熟石灰反应可以制得漂白粉,该反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O (7). Ca(ClO)2在空气中与二氧化碳和水反应会转化为CaCO3和HClO,该反应的化学方程式为Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO (8). 氧气的质量为34g+1g-34.2g=0.8g。 设过氧化氢溶液中溶质的质量为x,
2H2O2 MnO2 2H2O+O2↑
68 32
x 0.8g 68/x=32/0.8g x=1.7g
过氧化氢溶液中溶质的质量分数是1.7g÷34g×100%=5%
答:略

【题目】学习了酸和碱的化学性质后,同学们围绕“酸和碱的中和反应”开展了探究活动。请你参与学习并填写空格。
李军同学将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中,一会儿后,发现忘记了滴加指示剂。于是他从烧杯中取出少量反应后的溶液于试管中,滴入几滴酚酞溶液,振荡,观察到无明显现象。此中和反应的化学方程式为______________________。
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质组成是什么?
【假设猜想】针对疑问,大家纷纷提出猜想
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和_________
同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的是猜想______。
【实验探究】为了验证其余猜想,同学们利用烧杯中的溶液,进行如下方案的探究。
实验方案 | 实验现象 | 结论与解释 |
方案一:滴加Na2CO3溶液 | __________________ | 溶液中有H2SO4 |
方案二:滴加BaCl2溶液 | ____________ | 溶液中有H2SO4 |
【得出结论】通过探究,同学们一致确定猜想二是正确的。
【评价反思】老师对同学们能用多种方法进行探究给予了肯定,同时指出实验方案中有一个是错误的,错误的原因是_______________________________________________。