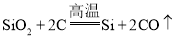题目内容
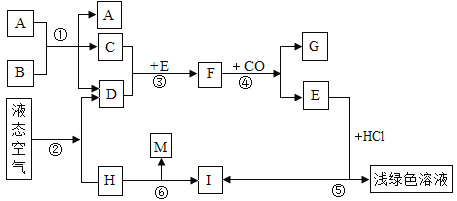
【题目】医疗上的生理盐水中含有A、B、C、D四种元素A、B、C、D的原子序数依次增大
(1)D元素的名称是______
(2)A与B可形成原子个数比1:1的分子,其化学式为_______,该分子中B的化合价是_______
(3)A、B、C形成化合物X的名称为________,其固体溶于水时要______(填“吸热”或“放热”),在X的水溶液中滴加少量CuSO4溶液,现象是_________,A与D形成化合物Y,Y与X在水溶液中反应的化学方程式为_________
【答案】氯元素 H2O2 -1 NaOH 放热 有蓝色絮状沉淀产生 HCl+NaOH=NaCl+H2O
【解析】
医疗上的生理盐水是氯化钠的水溶液,含有钠、氯、氢、氧四种元素,A、B、C、D的原子序数依次增大,则A、B、C、D分别是氢、氧、钠、氯四种元素。
(1)D元素的名称是氯元素;
(2)A与B可形成原子个数比1:1的分子,即为过氧化氢,其化学式为H2O2,氢元素显+1价,设氧元素的化合价是![]() ,根据在化合物中正负化合价代数和为零,可得:(+1)×2+2
,根据在化合物中正负化合价代数和为零,可得:(+1)×2+2![]() =0,则
=0,则![]() =-1价。该分子中B的化合价是-1价。
=-1价。该分子中B的化合价是-1价。
(3)A、B、C形成化合物X为氢氧化钠,其固体溶于水时放出大量的热,在氢氧化钠溶液中滴加少量CuSO4溶液,氢氧化钠和硫酸铜反应生成氢氧化铜蓝色沉淀,故现象是有蓝色絮状沉淀产生。A与D形成化合物Y,Y为HCl,Y与X(NaOH)在水溶液中反应生成氯化钠和水,化学方程式为HCl+NaOH=NaCl+H2O。

 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案【题目】氯酸钾有多种用途,常作氧化剂、火箭推进剂等,它易溶于水,在加热时可缓慢释放氧气,但在氧化铜等催化作用下加热会快速放出氧气。小华利用氯酸钾制取氧气来验证氧化铜的催化作用,并探究反应后剩余固体的成分。
(查阅资料)①氯化钾、氧化铜加热不分解;
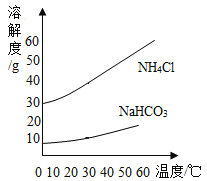
②硫酸铜易溶于水,溶解度随温度的升高而增大;
③![]()
I.催化剂的制备

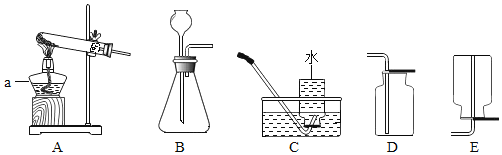
(1)步骤1的目的是除去不溶性杂质,步骤1所用到的玻璃仪器有_____。
(2)步骤2的目的是得到CuSO4.5H2O晶体,实验操作是_____、降温结晶、过滤、洗涤、干燥。
Ⅱ.加热氯酸钾制取氧气并探究剩余固体的成分
小华设计了以下两组实验,在相同条件下加热,并记录产生VL氧气所需要的时间,实验发现t1>t2,说明氧化铜可以加快氯酸钾的分解,相关数据如下表。
实验编号 | 反应前氯酸钾的质量 | 加入氧化铜的质量 | 生成VL 氧气所用的时间 | 反应后剩余固体的质量 |
ⅰ | 24.5g | 0 | t1 | m |
ⅱ | 24.5g | 2.0g | t2 | 21.7g |
(1)实验ⅰ中反应后剩余固体的质量m=_____。
(2)探究实验ⅱ反应后剩余固体的成分和氧化铜的催化作用,部分数据如下表。
实验步骤 | 现象或结论 |
①将反应后剩余固体继续加热,直至冷却后连续两次称量固体的质量保持不变。 | 若有气体生成,则说明含有氯酸钾,该反应的化学方程式为_____。 |
②将①加热后剩余固体在足量水中充分溶解,过滤、洗涤、干燥、称量 | 若滤渣的质量为_____,可进一步说明氧化铜对氯酸钾分解有催化作用。 |
③收集、合并②的滤液和洗涤液,加入过量硝酸银溶液,充分反应后过滤、洗涤、干燥、称量 | 理论上可得到沉淀的质量为_____。 |