题目内容
【题目】生铁和钢都是铁合金,生铁中碳的含量在2.0% -4.3%之间,钢中碳的含量在0.03% -2%之间。某兴趣小组同学取铁合金样品5.7g(假设只含铁单质及碳单质),加入稀硫酸至不再产生气体为止,反应过程中生成的气体与所加稀硫酸的质量关系如图所示。
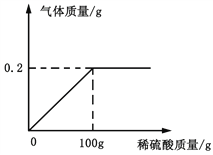
根据计算回答(计算结果保留一位小数):
(1)该铁合金是生铁还是钢?
(2)加入的稀硫酸中溶质的质量分数是多少?
【答案】(1)铁合金是钢;(2)9.8%
【解析】本题主要考查根据化学反应方程式的计算。由生成氢气的质量和铁合金的质量,根据铁与稀硫酸反应的化学方程式可以计算出铁合金中铁的质量,铁合金的质量与铁的质量之差就是铁合金中碳的质量,进而计算出量铁合金的含碳量,通过对比即可确定是生铁还是钢
解:设铁的质量为x,硫酸的质量为y
Fe+H2SO4=FeSO4+H2↑
56 98 2
X y 0.2g
56/2=x/0.2g
X=5.6g
98/2=y/0.2g
Y=9.8g
铁合金的含碳量为:(5.7g-5.6g)/5.7g×100%=1.76%
9.8g/100g×100%=9.8%
答:该铁合金是钢,稀硫酸中溶质的质量分数是1.76%

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目