题目内容
【题目】(10分)金属在生产和生活中有广泛的应用。
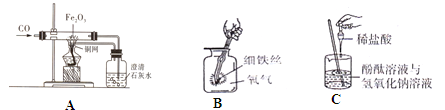
(1)下列铜制品中,利用金属导热性的是 (填字母序号)。

(2)铁制品在空气中易锈蚀,其实质是铁与空气中的氧气、 等接触后发生化学反应。
(3)已知金属M和N能够发生如下反应:M+H2SO4═MSO4+H2↑,Fe+MCl2═M+FeCl2,N+FeCl2═Fe+NCl2,判断Fe、Cu、M、N的活动性由强到弱的顺序是 .(2分)
(4)某兴趣小组在实验室发现了一块绿色的孔雀石标本,查阅资料知其主要成分是[mCu2 (OH)2 CO3。他们以Cu2 (OH)2 CO3原料制取铜,其工艺流程如下图所示:

①过滤操作中用到的铁制仪器为 。
②无色气体A的化学式是 ,大气中该气体含量不断上升,会导致增强,全球气候变暖。
③写出蓝色溶液B与铁粉反应的化学方程式 。(2分)试剂E可选用 溶液。
【答案】(1)C (1分)
(2)水(H2O)(1分)
(3)N >Fe >M >Cu (2分)
(4)①铁架台(1分) ②CO2 (1分) 温室效应 (1分)
③Fe + CuSO4 = FeSO4 + Cu (2分)稀盐酸(或稀硫酸等)(1分)
【解析】
试题分析:(1)铜火锅利用了金属的导热性;
(2)铁生锈是铁与空气中的氧气和水蒸气共同作用;
(3)M+H2SO4═MSO4+H2↑可得M﹥H,Fe+MCl2═M+FeCl2可得Fe>M,N+FeCl2═Fe+NCl2,可得N﹥Fe,又Cu﹤H,综上N >Fe >M >Cu;
(4)①为铁架台;②Cu2(OH)2 CO3含有碳酸根,与酸反应生成气体为二氧化碳;③与硫酸反应后得到的蓝色溶液推测为硫酸铜,因此是硫酸铜与铁的反应;过滤后固体为Cu和多余的Fe,加入的试剂只与Fe反应且有气体生成,那么E是酸,可以是盐酸或硫酸。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案