题目内容
【题目】洁厕灵是常用的陶瓷清洗液,小鑫同学对某品牌洁厕灵的有效成分及其含量进行研究。
(1)查阅资料得知:洁厕灵有效成分是HCl.HCl与NaHCO3反应的化学方程式:HCl+NaHCO3=NaCl+H2O+CO2↑,洁厕灵中其它成分均不参与反应。
(2)向一锥形瓶中加入100克该品牌的洁厕灵,再加入溶质质量分数7%的NaHCO3溶液120g,恰好完全反应,反应后溶液的总质量是215.6g。试计算下列问题:
①根据质量守恒定律产生的二氧化碳质量为______克。
②所加NaHCO3溶液中溶质质量是______克。
③该品牌洁厕灵中HCl的质量分数是_________________?
【答案】4.4 8.4 7.3%
【解析】
盐酸和碳酸氢钠反应生成氯化钠和水和二氧化碳,根据质量守恒定律参加反应的反应物的总质量等于生成的生成物的总质量。
根据质量守恒定律可得,生成的二氧化碳的质量为100g+120g-215.6g=4.4g
设所加NaHCO3溶液中溶质质量为x,洁厕灵中HCl的质量分数为y
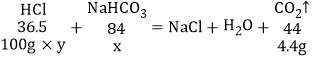
![]()
x=8.4g y=7.3%

练习册系列答案
相关题目
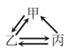
【题目】下列各组转化关系中的反应为初中化学常见的反应,其中的“→”表示某种物质可一步反应生成另一种物质。甲、乙、丙三种物质不符合对应“转化关系”的是
选项 | A | B | C | D | |
转化关系 |
|
|
|
| |
物质 | 甲 | H2O2 | C | CaCO3 | FeCl2 |
乙 | O2 | CO | CO2 | Fe | |
丙 | H2O | CO2 | Na2CO3 | Fe2O3 | |