题目内容
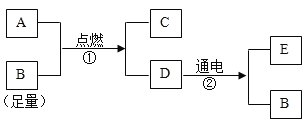
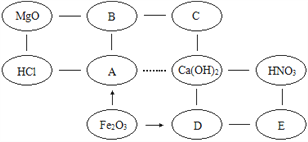
【题目】从微观视角看物质的变化是化学研究的内容之一.下图分别表示生成氯化钠的不同化学反应.请根据图示回答相关问题:

(1)由图甲可知,反应中得到电子的是________原子;钠元素在元素周期表中的位置位于第_____________周期.
(2)由图乙可知,NaOH溶液与盐酸反应的微观实质是________________.
(3)图丙表示反应的化学方程式为________;NaClO2中氯的化合价是_______.
(4)由图可知氯化钠是由________(填“离子”、“分子”、“原子”)构成;锶元素(元素符号为Sr)的原子最外层电子数为2,则氯化锶的化学式为______.
【答案】 氯原子 三 氢离子与氢氧根离子结合生成水分子 Cl2+2NaClO2=2ClO2+2NaCl +3 离子 SrCl2
【解析】根据微观示意图及化学式、化学方程式的书写解答;化学式中正负化合价代数和为0分析解答。
解:(1)由图甲可知,氯原子的最外层电子数为7,得到电子形成最外层为8个的相对稳定结构。故反应中得到电子的是氯原子;由图甲可知,钠原子核外有3个电子层,故钠元素在元素周期表中的位置位于第三周期;
(2)由图乙可知,氢氧化钠解离成Na+和A,则A是OH-。HCl解离成Cl-和B。则B是H+。A和B结合为C,则C是水。即NaOH溶液与盐酸反应的微观实质是:氢离子与氢氧根离子结合生成水分子。
(3)图丙表示的是次氯酸钠和氯气反应生成次氯酸和氯化钠,反应的化学方程式为:Cl2+2NaClO2=2ClO2+2NaCl;NaClO2中钠元素显+1价,氧元素显-2价,因此氯元素的化合价为0-(+1)-(-2×2)=+3价。
(4)由图可知氯化钠是由钠离子和氯离子构成。故填:离子;锶元素(元素符号为Sr)的原子最外层电子数为2,通常显+2价,又氯元素显-1价,所以氯化锶的化学式为:SrCl2。