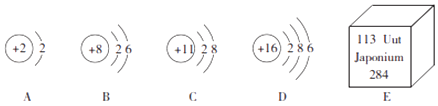题目内容
【题目】下列物质是混合物的是
A.海水 B.液氮 C.金属铜 D.冰水混合物
【答案】A
【解析】
试题分析:A、含有水、食盐氯化钠等多种物质,混合物;B、含有氮气一种物质,纯净物;C、含有铜一种物质,纯净物;D、含有水一种物质,纯净物。

【题目】某研究小组欲检验草酸晶体样品分解产物并测定其质量分数(假设杂质不参与反应).草酸晶体(H2C2O42H2O)的理化性质见表.
(1)加热分解草酸晶体最适宜的装置是(填图1字母序号). 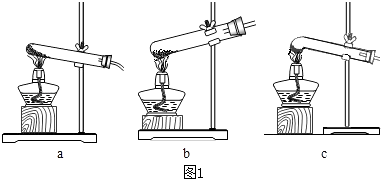
(2)图2是验证热分解产物中含CO,CO2的装置 ①仪器a和b的名称分别是和
②证明存在CO2的现象是 , 证明存在CO的现象是 , D中反应的化学方程式是 .
③装置A的作用是 , 气囊的作用是 . 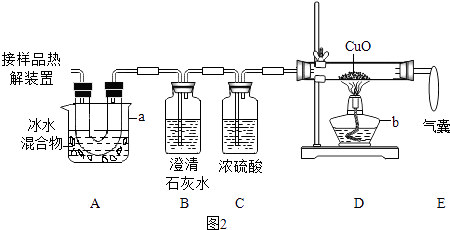
(3)为测定样品中草酸晶体的质量分数,设计两种如下方案.
熔点 | 沸点 | 热稳定性 | 与碱反应 |
101°C~102°C | 150°C~160°C升华 | 100.1°C失去结晶水,175°C分解成CO2 , CO,H2O | 与Ca(OH)2反应产生白色沉淀(CaC2O4) |
①称一定量样品用上图装置进行实验,测得装置D反应前后的质量差,由此计算出的实验结果比实际值偏低,排除仪器和操作的因素,其原因可能有:CO未完全反应、 .
②称取8.75g草酸晶体样品配制50.00g溶液,取10.00g溶液加适量的稀硫酸,然后滴加25.00g3.16%KMnO4溶液,恰好反应完全.
(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)则KMnO4溶液显色,25.00g3.16%KMnO4溶液中KMnO4的质量g.请计算样品中的质量分数.[写出计算过程,M2(H2C2O4)=90,M2(H2C2O42H2O)=126,M2(KMnO4)=158].