题目内容
【题目】下列说法正确的是( )
A. 等质量的CO和CO2中氧元素的质量比为11∶14
B. 等质量的Al和Mg分别与足量稀硫酸充分反应,生成H2的质量相等
C. 等质量的NaHCO3和MgCO3分别与足量稀盐酸充分反应,生成CO2的质量相等
D. 等质量的溶质质量分数均为4%氢氧化钠溶液与稀盐酸充分反应后,所得溶液显中性
【答案】AC
【解析】
A、设CO和CO2的质量为m,则等质量的CO和CO2中所含氧元素的质量比是![]() ,故A正确;B、根据化学方程式2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑,Mg + H2SO4 = MgSO4 + H2↑可知,Al的相对原子质量为27,27g铝可反应生成3g氢气,即1g铝生成1/9g氢气,Mg的相对原子质量为24,24g镁可反应生成2g氢气,即1g镁生成1/12g氢气,铝产生的氢气质量大于镁,故B错误;C、根据化学方程式NaHCO3+HCl==NaCl+H2O+CO2和MgCO3+2HCl==MgCl2+H2O+CO2↑,可知,每84份质量的NaHCO3能生成44份质量的二氧化碳,每84份质量的MgCO3能生成44份质量的二氧化碳,可以判断生成二氧化碳气体的质量相等,故C相等;D、反应中消耗盐酸与氢氧化钠的质量比关系为:
,故A正确;B、根据化学方程式2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑,Mg + H2SO4 = MgSO4 + H2↑可知,Al的相对原子质量为27,27g铝可反应生成3g氢气,即1g铝生成1/9g氢气,Mg的相对原子质量为24,24g镁可反应生成2g氢气,即1g镁生成1/12g氢气,铝产生的氢气质量大于镁,故B错误;C、根据化学方程式NaHCO3+HCl==NaCl+H2O+CO2和MgCO3+2HCl==MgCl2+H2O+CO2↑,可知,每84份质量的NaHCO3能生成44份质量的二氧化碳,每84份质量的MgCO3能生成44份质量的二氧化碳,可以判断生成二氧化碳气体的质量相等,故C相等;D、反应中消耗盐酸与氢氧化钠的质量比关系为: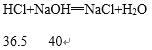 ,所以36.5份质量的盐酸与40份质量的氢氧化钠恰好完全反应,等质量、等质量分数的盐酸和氢氧化钠两种溶液充分混合后,稀盐酸有剩余,溶液显酸性,故D错误。故选AC。
,所以36.5份质量的盐酸与40份质量的氢氧化钠恰好完全反应,等质量、等质量分数的盐酸和氢氧化钠两种溶液充分混合后,稀盐酸有剩余,溶液显酸性,故D错误。故选AC。

 特高级教师点拨系列答案
特高级教师点拨系列答案【题目】四种物质在密闭容器内充分反应,测得反应前后各物质的质量分数如下表所示。则有关说法中错误的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前 | 17% | 10% | 25% | 48% |
反应后 | 19% | 10% | 41% | 30% |
A. 丁一定是化合物
B. 乙可能是这个反应的催化剂
C. 该反应可以是碳酸钙或过氧化氢的分解反应
D. 参加反应的丁的质量一定等于生成甲和丙的质量之和