题目内容
【题目】如图是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A,B,C均为氧化物,常温下B为液态.化合物D的水溶液呈浅绿色. 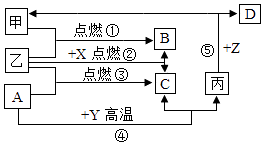
(1)写出有关物质的化学式:X;
(2)指出反应④在生产实际中的应用:(举一例说明);
(3)写出下列反应的化学方程式:④ . ⑤ .
【答案】
(1)CH4
(2)工业炼铁
(3)3CO+Fe2O3![]() 2Fe+3CO2 (Fe3O4等亦可);Fe+2HCl═FeCl2+H2↑ (H2SO4亦可)
2Fe+3CO2 (Fe3O4等亦可);Fe+2HCl═FeCl2+H2↑ (H2SO4亦可)
【解析】解:(1)化合物D的水溶液呈浅绿色和框图中转化,D中含有Fe2+离子,因为甲、乙为气态单质,丙为固态单质,则丙为铁,甲为氢气,Z为酸;氧化物A能够和Y反应产生单质铁,因此A是一氧化碳,Y为铁的氧化物,C为二氧化碳;一氧化碳和乙点燃产生二氧化碳,因此乙为氧气;X和氧气点燃产生二氧化碳和水,因此X中含有碳元素和氢元素,可以是甲烷;(2)因反应④是CO还原铁的氧化物的反应产生铁,可用于工业上冶炼(生)铁;(3)根据转化可知反应④炼铁的原理,可以是:3CO+Fe2O3 ![]() 2Fe+3CO2 (Fe3O4等亦可);⑤是铁和酸反应制氢气,可以为:Fe+2HCl═FeCl2+H2↑ (H2SO4亦可);所以答案是:(1)CH4;(2)工业炼铁;(3)④3CO+Fe2O3
2Fe+3CO2 (Fe3O4等亦可);⑤是铁和酸反应制氢气,可以为:Fe+2HCl═FeCl2+H2↑ (H2SO4亦可);所以答案是:(1)CH4;(2)工业炼铁;(3)④3CO+Fe2O3 ![]() 2Fe+3CO2 (Fe3O4等亦可);⑤Fe+2HCl═FeCl2+H2↑ (H2SO4亦可).
2Fe+3CO2 (Fe3O4等亦可);⑤Fe+2HCl═FeCl2+H2↑ (H2SO4亦可).
【考点精析】根据题目的已知条件,利用书写化学方程式、文字表达式、电离方程式的相关知识可以得到问题的答案,需要掌握注意:a、配平 b、条件 c、箭号.

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案【题目】硝酸钾的溶解度如下图所示,有关叙述正确的是( )
温度(℃) | 20 | 30 | 40 | 50 | 60 |
溶解度(g/100g水) | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
A.20℃时,可配成50g35%的硝酸钾饱和溶液
B.30℃和50℃时,等质量的硝酸钾饱和溶液,所含水的体积,前者大于后者
C.40℃时,50g硝酸钾饱和溶液降温至20℃,析出固体的质量为32.3g
D.60℃时,50g硝酸钾饱和溶液中,溶质与溶剂的质量比为11:21