题目内容
金属是人类生活中的常用的材料.
(1)下列生活用品中,主要利用金属导热性的是 (填字母序号).
(2)工业上用赤铁矿(主要成分是氧化铁)冶炼铁的化学方程式是 .
(3)现有锌片、铜片、稀硫酸、硫酸锌溶液和硫酸铜溶液5种物质,某同学欲探究锌和铜的金属活动性顺序,选择的一组试剂是 ,其现象是 .
(4)该同学查阅资料得知,铜锈的主要成分是碱式碳酸铜【Cu2(OH)2CO3】,他以铜锈为原料设计并完成如下实验(杂质不与稀硫酸反应,且不含铜元素.图中部分物质略去).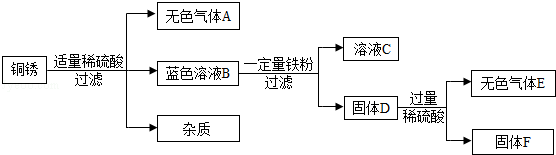
①溶液C中所含的溶质是 .
②已知铜锈中Cu2(OH)2CO3的质量分数是10%,固体F的质量是1.28g,则铜锈中含Cu的质量分数是
(结果精确至0.1%).
(1)AB;(2)3CO+Fe2O3 2Fe+3CO2;(3)锌片、铜片、稀硫酸 锌片与稀硫酸反应有气体放出,铜片与稀硫酸没有气体放出;(4)①FeSO4 ②5.8%.
2Fe+3CO2;(3)锌片、铜片、稀硫酸 锌片与稀硫酸反应有气体放出,铜片与稀硫酸没有气体放出;(4)①FeSO4 ②5.8%.
解析试题分析:(1)铁锅是利用金属的导热性,铜制火锅是利用金属的导热性,铝制易拉罐是利用金属的延展性;(2)一氧化碳具有还原性,能与氧化铁反应生成铁和二氧化碳,故填:3CO+Fe2O3 2Fe+3CO2;(3)要设计实验验证锌和铜的活动性强弱,可以利用锌在氢前而铜在氢后,氢前金属能与稀硫酸反应产生氢气,而氢后金属不能与稀硫酸反应产生氢气的性质设计实验选择试剂,故填:锌片、铜片、稀硫酸 锌片与稀硫酸反应有气体放出,铜片与稀硫酸没有气体放出;(4)铜锈能与稀硫酸反应生成二氧化碳和硫酸铜,硫酸铜能与铁反应生成硫酸亚铁和铜,故C中一定含有硫酸亚铁,得到的固体D能与酸反应生成气体,则D中含有铁和铜,得到的固体F是铜,在一个碱式碳酸铜分子中含有两个铜原子,故其质量关系为Cu2(OH)2CO3﹣﹣2Cu,设碱式碳酸铜的质量为x
2Fe+3CO2;(3)要设计实验验证锌和铜的活动性强弱,可以利用锌在氢前而铜在氢后,氢前金属能与稀硫酸反应产生氢气,而氢后金属不能与稀硫酸反应产生氢气的性质设计实验选择试剂,故填:锌片、铜片、稀硫酸 锌片与稀硫酸反应有气体放出,铜片与稀硫酸没有气体放出;(4)铜锈能与稀硫酸反应生成二氧化碳和硫酸铜,硫酸铜能与铁反应生成硫酸亚铁和铜,故C中一定含有硫酸亚铁,得到的固体D能与酸反应生成气体,则D中含有铁和铜,得到的固体F是铜,在一个碱式碳酸铜分子中含有两个铜原子,故其质量关系为Cu2(OH)2CO3﹣﹣2Cu,设碱式碳酸铜的质量为x
Cu2(OH)2CO3﹣﹣2Cu
222 128
x 1.28g x=2.22g
x=2.22g
则铜锈的质量为: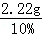 =22.2g
=22.2g
故铜锈中铜元素的质量分数为: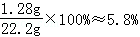 ;故填:①FeSO4 ②5.8%.
;故填:①FeSO4 ②5.8%.
考点:金属的物理性质及用途;金属活动性顺序及其应用;一氧化碳还原氧化铁.

人类的生活和生产都离不开金属材料。
(1)金属以矿物形式存在,下列矿石的主要成分属于氧化物的是_______(填化学式)。
(2)铁是应用最广泛的金属。
①下列金属制品的用途中,利用金属导热性的是 (填字母序号)。
②还原铁粉又称“双吸剂”,常用于食品保鲜,其原理是:______________________________________。
③下列说法正确的是 。
| A.来铁和铁合金都容易被锈蚀 |
| B.回收废旧金属有利于节约金属资源 |
| C.铁丝在氧气中剧烈燃烧,火星四射,生成氧化铁 |
| D.在铁桶中加入硫酸铜溶液和石灰乳来配制农药波尔多液 |

请回答:
①固体B的成分是 。
②检验C过量的方法是 。
人类的生产和生活都离不开金属.
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是 .金属以矿物形式存在,下列矿石的主要成分属于氧化物的是 (填化学式).
赤铁矿 孔雀石 铝土矿
(主要成分Fe2O3)〔主要成分Cu2(OH)2CO3〕(主要成分Al2O3)
(2)金属的回收和利用是保护金属资源的一种有效途径.
①废钢铁可回收重新冶炼,用一氧化碳还原氧化铁的化学方程式为 .
②向含有AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一定量的铁粉,使其充分反应后,过滤,向滤渣中滴加稀盐酸,有气泡产生,则下列结论正确的是
| A.固体中一定有Fe、Ag,可能有 Cu、Zn |
| B.固体中一定有Fe、Zn,可能有 Cu、Ag |
| C.滤液中一定含Fe2+、Zn2+,不含Cu2+、Ag+ |
| D.滤液中一定含Zn2+、Fe2+,可能含Cu2+ |

请回答:
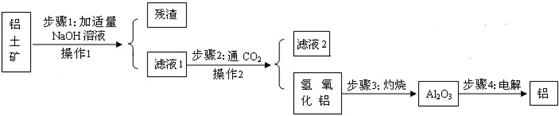
①操作1的名称是 ;固体A的成分为 .
②若要检验向固体C中加入的稀硫酸是否足量的方法是 .
③若实验过程中的物质损失可以忽略,要计算该废液中硫酸锌的质量分数,必须称量废液的质量、蒸发得到固体硫酸锌的质量和 ..