题目内容
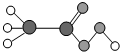 2003年我国部分地区突发“非典”,严重危害人体健康.为防治“非典”,对公共场所进行消毒时常用过氧乙酸消毒液,过氧乙酸的分子结构如图所示:其中
2003年我国部分地区突发“非典”,严重危害人体健康.为防治“非典”,对公共场所进行消毒时常用过氧乙酸消毒液,过氧乙酸的分子结构如图所示:其中 代表碳原子,
代表碳原子, 代表氢原子,
代表氢原子, 代表氧原子.则:过氧乙酸的化学式为
代表氧原子.则:过氧乙酸的化学式为过氧乙酸中碳、氢、氧元素的质量比为:
过氧乙酸中碳元素质量分数为
考点:化学式的书写及意义,相对分子质量的概念及其计算,元素质量比的计算,元素的质量分数计算
专题:化学用语和质量守恒定律
分析:根据物质的微观构成可以判断物质的化学式,根据化学式可以计算相对分子质量、元素质量比、元素质量分数等.
解答:解:由图中可知,过氧乙酸的化学式为:C2H4O3,化学式量为:12×2+1×4+16×3=76.
过氧乙酸中碳、氢、氧三种元素的质量比是 (12×2):(1×4):(16×3)=24:4:48=6:1:12.
过氧乙酸中碳元素的质量分数是
×100%≈31.6%.
故答案为:C2H4O3;76;6:1:12;31.6%.
过氧乙酸中碳、氢、氧三种元素的质量比是 (12×2):(1×4):(16×3)=24:4:48=6:1:12.
过氧乙酸中碳元素的质量分数是
| 12×2 |
| 12×2+1×4+16×3 |
故答案为:C2H4O3;76;6:1:12;31.6%.
点评:本题主要考查了物质的化学式及其根据化学式进行相关方面计算的知识.

练习册系列答案
相关题目
化合物XY和ZY2中Y的质量分数分别为40%与50%,则化合物XZY4中X的质量分数为( )
| A、20% | B、30% |
| C、40% | D、50% |
下列说法正确的是( )
| A、NaOH和MgO的混合物中氧的质量分数为40%,NaOH和MgO的质量比为任意值 |
| B、一定量的氯化钠溶液恒温蒸发5克水,析出a克晶体;再蒸发5克水,又析出b克晶体,a与b一定相等 |
| C、用H2完全还原一定质量的CuO,参加反应的H2与通入的H2质量一定相等 |
| D、将98%的浓H2SO4稀释成49%的稀H2SO4,加入水的质量与浓硫酸质量一定相等 |
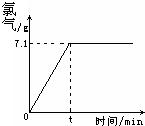 取氯化钠溶液117g进行电解,反应的化学方程式为:2NaCl+2H2O═Cl2↑+H2↑+2NaOH,生成氯气的质量与时间的关系如图所示.请计算:
取氯化钠溶液117g进行电解,反应的化学方程式为:2NaCl+2H2O═Cl2↑+H2↑+2NaOH,生成氯气的质量与时间的关系如图所示.请计算: