题目内容
(1)硫酸铵的化学式是 ,相对分子质量是 ,硫酸铵中氮元素的质量分数是 (最终结果保留小数后一位)
(2)已知一个碳-12原子的质量是a kg,如果另一种A原子的质量为b kg,且每个A原子中有c个质子,求A原子的相对原子质量是 , A原子核内的中子数是
(1) (NH4)2SO4 ;132;36.9%. (2) 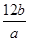 ;
;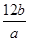 ?c
?c
解析试题分析:(1)化合物化学式的书写一般规律:先读后写,后读先写;金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零,故硫酸铵的化学式为: ;相对分子质量等于组成分子的各个原子的相对原子质量之和故硫酸铵的相对分子质量为:(14+1*4)*2+32+16*4=132;硫酸铵中氮元素的质量分数为:  ×100%,故硫酸铵氮元素的质量分数为:
×100%,故硫酸铵氮元素的质量分数为: ×100%=36.9%.
×100%=36.9%.
(2)弄清相对原子质量的概念,然后根据相对原子质量的计算公式以及原子中质子数与中子数之和约等于相对原子质量分析解答即可.由于相对原子质量= ,故A的相对原子质量为
,故A的相对原子质量为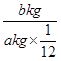 =
=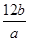 ;而原子中质子数与中子数之和约等于原子的相对原子质量,所以该原子的中子数为
;而原子中质子数与中子数之和约等于原子的相对原子质量,所以该原子的中子数为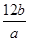 ?c.
?c.
考点:化学式的书写及意义;相对分子质量的概念及其计算;元素的质量分数计算;原子的有关数量计算.

练习册系列答案
相关题目
下列关于原子核的叙述中,正确的是( )
①通常由中子和电子构成 ②通常由质子和中子构成 ③带负电荷 ④不显电性 ⑤不能再分 ⑥体积大约相当于原子 ⑦质量大约相当于原子
| A.①⑤ | B.②⑦ | C.③④ | D.②⑥⑦ |
“对比实验”是化学学习中行之有效的思维方法。某化学学习小组的同学在学完相关的化学知识后,走进实验室做了如下实验,请你参与并回答下列问题。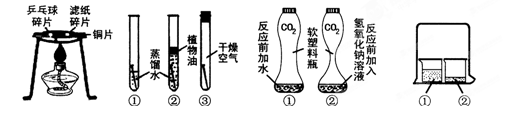
| A.燃烧的条件 | B.铁钉生锈的条件 | C.证明CO2与NaOH反应 | D.分子运动的现象 |
(2)对于实验B,一段时间后观察到试管①中的铁钉明显锈蚀,由此得出:铁生锈的主要条件是铁与水和 直接接触。若用稀硫酸来除去铁制品表面的铁锈, (填“能”或“不能”)长时间浸在稀硫酸溶液中,理由是 (用化学方程式表示)。
(3)实验C是利用体积相同并充满CO2的软塑料瓶、等量的水(瓶①)和NaOH溶液(瓶②)进行实验,根据塑料瓶变瘪的程度证明CO2与NaOH溶液中的溶质确实发生了反应,这一反应的化学方程式为 。
(4)实验D的烧杯②中呈现的现象能说明分子是不断运动的。当烧杯①中液体是浓氨水时烧杯②中的酚酞溶液由无色变为 色;当烧杯①中液体换成浓盐酸,且烧杯②中液体换成滴有酚酞的NaOH溶液时,一段时间后,溶液颜色的变化是 。其中盐酸与NaOH反应的化学方程式 。