题目内容
化学兴趣小组同学发现实验台上按如下顺序摆放着7瓶不同的无色溶液(如图所示),其中4、5号试剂瓶标签破损.?

[提出问题]这两瓶试剂分别是什么??
[查阅资料]
①碱性的亚硫酸钠(Na2SO3)溶液、Na2CO3溶液都能与中性的CaCl2溶液发生复分解反应,产生白色沉淀.②Na2SO3+2HCl=2NaCl+SO2↑+H2O.?
③CO2与SO2均可以使澄清石灰水变浑浊,SO2是一种有刺激性气味的气体.?
[作出猜想]4、5号溶液可能分别是NaOH、Na2CO3、Na2SO3或NaCl溶液中的一种.
[实施方案]取少量4、5号溶液分别于试管中,然后分别进行下列三组实验.?
实验1:在两支试管中分别滴入上述七种溶液中的
实验3:在两支试管中分别滴入上述七种溶液中的2号溶液,在盛4号溶液的试管中有
[实验反思]同学们经过分析,认为4号溶液还可能是变质的NaOH溶液.请你利用上述图中的试剂设计鉴定实验方案,完成实验报告.
25.(5分)某化学兴趣小组的同学参照教科书内容,在学校实验室里完成了以下两个实验:
实验一:配制溶质质量分数为6%的NaCl溶液50g,按如下步骤进行操作:
实验二:称取5.0g粗盐进行提纯.粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质.为了有效将粗盐提纯,实验的各步操作流程如图2所示:

请你根据以上信息回答下述问题:
(1)配制50g溶质质量分数为6%的NaCl溶液,需NaCl
(2)NaCl溶解过程用到了玻璃棒,它的作用是
(3)粗盐提纯时,操作I的名称为
(4)某同学所得精盐比其他同学明显要少,原因可能是
A.溶解时将5.0g粗盐一次全部倒入水中,立即过滤
B.蒸发时有一些液体、固体溅出
C.提纯后所得精盐尚未完全干燥.

[提出问题]这两瓶试剂分别是什么??
[查阅资料]
①碱性的亚硫酸钠(Na2SO3)溶液、Na2CO3溶液都能与中性的CaCl2溶液发生复分解反应,产生白色沉淀.②Na2SO3+2HCl=2NaCl+SO2↑+H2O.?
③CO2与SO2均可以使澄清石灰水变浑浊,SO2是一种有刺激性气味的气体.?
[作出猜想]4、5号溶液可能分别是NaOH、Na2CO3、Na2SO3或NaCl溶液中的一种.
[实施方案]取少量4、5号溶液分别于试管中,然后分别进行下列三组实验.?
实验1:在两支试管中分别滴入上述七种溶液中的
1
1
号溶液,两试管中的溶液均变成红色,说明4、5号溶液均不可能是上述猜想中的NaCl
NaCl
溶液.?实验2:在两支试管中分别滴入上述七种溶液中的3号溶液,两试管中均产生白色沉淀,4、5号溶液可能分别是Na2SO3溶液和Na2CO3溶液中的一种.写出其中一个反应的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
(或Na2SO3+Ca(OH)2═CaSO3↓+2NaOH)
(或Na2SO3+Ca(OH)2═CaSO3↓+2NaOH)
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
(或Na2SO3+Ca(OH)2═CaSO3↓+2NaOH)
.(或Na2SO3+Ca(OH)2═CaSO3↓+2NaOH)
实验3:在两支试管中分别滴入上述七种溶液中的2号溶液,在盛4号溶液的试管中有
无色无味的气体产生
无色无味的气体产生
现象,说明4号是Na2CO3溶液;在盛5号溶液的试管中有刺激性气味的气体产生
刺激性气味的气体产生
现象,说明5号是Na2SO3溶液.[实验反思]同学们经过分析,认为4号溶液还可能是变质的NaOH溶液.请你利用上述图中的试剂设计鉴定实验方案,完成实验报告.
| 实验操作 | 实验现象 | 实验结论 |
4号溶液是部分变质的NaOH溶液. |
实验一:配制溶质质量分数为6%的NaCl溶液50g,按如下步骤进行操作:
实验二:称取5.0g粗盐进行提纯.粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质.为了有效将粗盐提纯,实验的各步操作流程如图2所示:

请你根据以上信息回答下述问题:
(1)配制50g溶质质量分数为6%的NaCl溶液,需NaCl
3
3
g,水47
47
mL.(2)NaCl溶解过程用到了玻璃棒,它的作用是
搅拌,加速溶解
搅拌,加速溶解
.(3)粗盐提纯时,操作I的名称为
过滤
过滤
.(4)某同学所得精盐比其他同学明显要少,原因可能是
AB
AB
.A.溶解时将5.0g粗盐一次全部倒入水中,立即过滤
B.蒸发时有一些液体、固体溅出
C.提纯后所得精盐尚未完全干燥.
分析:【实施方案】实验1:酚酞遇碱性溶液变红,而与酸性和中性溶液不变色,可以据此解答;
实验2:根据查阅资料部分可以知道碳酸钠和亚硫酸钠都能够和氢氧化钙反应,根据复分解发生的条件可以知道,这两个反应都能生产沉淀,可以据此解答;
实验3:碳酸钠可以和盐酸反应生成无色无味的二氧化碳气体,而亚硫酸钠可以和盐酸反应生成有刺激性气味的二氧化硫气体,可以据此解答该题;
【实验反思】若氢氧化钠溶液部分变质,则可以在排除碳酸钠干扰的条件下用无色酚酞试液来进行检验;
25.(1)根据溶质质量=溶液质量×溶质质量分数,溶剂质量=溶液质量-溶质质量计算;(2)根据溶解时玻璃棒的作用考虑;(3)根据泥沙不溶于水来考虑;(4)根据溶解时将5.0g粗盐一次全部倒入水中,立即过滤有没溶解的考虑,固体溅出的后果,提纯后所得精盐尚未完全干燥的后果考虑.
实验2:根据查阅资料部分可以知道碳酸钠和亚硫酸钠都能够和氢氧化钙反应,根据复分解发生的条件可以知道,这两个反应都能生产沉淀,可以据此解答;
实验3:碳酸钠可以和盐酸反应生成无色无味的二氧化碳气体,而亚硫酸钠可以和盐酸反应生成有刺激性气味的二氧化硫气体,可以据此解答该题;
【实验反思】若氢氧化钠溶液部分变质,则可以在排除碳酸钠干扰的条件下用无色酚酞试液来进行检验;
25.(1)根据溶质质量=溶液质量×溶质质量分数,溶剂质量=溶液质量-溶质质量计算;(2)根据溶解时玻璃棒的作用考虑;(3)根据泥沙不溶于水来考虑;(4)根据溶解时将5.0g粗盐一次全部倒入水中,立即过滤有没溶解的考虑,固体溅出的后果,提纯后所得精盐尚未完全干燥的后果考虑.
解答:解:【实施方案】实验1:酚酞遇碱性溶液变红,而与酸性和中性溶液不变色,其中氢氧化钠溶液、碳酸钠溶液、亚硫酸钠溶液都能够使酚酞变红,只有氯化钠溶液呈中性,不会使酚酞变色,故该物质不可能是氯化钠溶液;
实验2:根据查阅资料部分可以知道碳酸钠和亚硫酸钠都能够和氢氧化钙反应,根据复分解发生的条件可以知道,这两个反应都能生产沉淀,它们反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH(或Na2SO3+Ca(OH)2═CaSO3↓+2NaOH);
实验3:碳酸钠可以和盐酸反应生成无色无味的二氧化碳气体,而亚硫酸钠可以和盐酸反应生成有刺激性气味的二氧化硫气体,所以若反应现象为产生无色无味的气体则该物质是碳酸钠,若产生有刺激性气味的气体,则是亚硫酸钠;
【实验反思】取4号溶液于试管中,加入足量的氯化钙溶液,如果产生白色沉淀,则证明有碳酸钠存在;然后取上层清液,加入无色酚酞试液,如果溶液变为红色,则可以判断该物质为部分变质的氢氧化钠溶液.
25.(1)氯化钠:50g×6%=3g,需要水:50g-3g=47g,体积:
=47ml;
(2)NaCl溶解过程用到了玻璃棒,是为了搅拌加速氯化钠溶解的;
(3)泥沙不溶于水,将不溶于液体的固体与液体分离的方法是过滤;
(4)溶解时将5.0g粗盐一次全部倒入水中,立即过滤,有没溶解的氯化钠被过滤掉了,所以所得精盐少了;蒸发时有一些液体、固体溅出,会导致氯化钠减少,所得精盐比其他同学明显要少;提纯后所得精盐尚未完全干燥,只能导致质量增多;
故答案为:【实验方案】实验1:1;NaCl(或氯化钠);
实验2:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(或Na2SO3+Ca(OH)2═CaSO3↓+2NaOH);
实验3:无色无味气体产生;刺激性气味的气体产生;
[实验反思]
25.(1)3;47;(2)搅拌,加速溶解;(3)过滤;(4)AB.
实验2:根据查阅资料部分可以知道碳酸钠和亚硫酸钠都能够和氢氧化钙反应,根据复分解发生的条件可以知道,这两个反应都能生产沉淀,它们反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH(或Na2SO3+Ca(OH)2═CaSO3↓+2NaOH);
实验3:碳酸钠可以和盐酸反应生成无色无味的二氧化碳气体,而亚硫酸钠可以和盐酸反应生成有刺激性气味的二氧化硫气体,所以若反应现象为产生无色无味的气体则该物质是碳酸钠,若产生有刺激性气味的气体,则是亚硫酸钠;
【实验反思】取4号溶液于试管中,加入足量的氯化钙溶液,如果产生白色沉淀,则证明有碳酸钠存在;然后取上层清液,加入无色酚酞试液,如果溶液变为红色,则可以判断该物质为部分变质的氢氧化钠溶液.
25.(1)氯化钠:50g×6%=3g,需要水:50g-3g=47g,体积:
| 47g |
| 1g/ml |
(2)NaCl溶解过程用到了玻璃棒,是为了搅拌加速氯化钠溶解的;
(3)泥沙不溶于水,将不溶于液体的固体与液体分离的方法是过滤;
(4)溶解时将5.0g粗盐一次全部倒入水中,立即过滤,有没溶解的氯化钠被过滤掉了,所以所得精盐少了;蒸发时有一些液体、固体溅出,会导致氯化钠减少,所得精盐比其他同学明显要少;提纯后所得精盐尚未完全干燥,只能导致质量增多;
故答案为:【实验方案】实验1:1;NaCl(或氯化钠);
实验2:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(或Na2SO3+Ca(OH)2═CaSO3↓+2NaOH);
实验3:无色无味气体产生;刺激性气味的气体产生;
[实验反思]
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量4号溶液于试管中,加入足量CaCl2溶液 | ①有白色沉淀生成 | 4号溶液是部分变质的NaOH溶液. |
| ②向上层清液中滴加无色酚酞试液 | ②溶液由无色变成红色 |
点评:要想解答好这类题目,首先,要理解和熟记物质的鉴别、推断及其方法,以及与之相关的知识.然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生产或生活经验所得,细致地分析题意(或实验、图表信息)等,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 (2009?德城区)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如下图所示.
(2009?德城区)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如下图所示.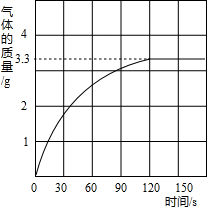 某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如图所示.
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢中,产生CO2气体的情况如图所示.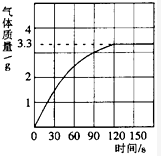 某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到10g水垢中,产生CO2气体的情况如图所示.
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到10g水垢中,产生CO2气体的情况如图所示.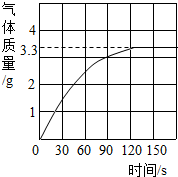 (2012?荔湾区一模)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到10g水垢中,产生CO2气体的情况如图所示.
(2012?荔湾区一模)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到10g水垢中,产生CO2气体的情况如图所示. 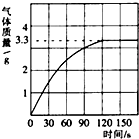 某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢后,产生CO2气体的情况如图所示.
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢后,产生CO2气体的情况如图所示.