��Ŀ����
����Ŀ��ij��ѧ�С����������ε�������Ϊ�������̽����ѧϰ��������Ϊ��С���Աһ��������������⣺
(1)С��ͬѧ��ijһǷ��ũ����ȡ��һ��������Ʒ���������������ԣ��Ӿ��úͿ��з��濼�ǣ���ôҪ���������������ԣ�Ӧ��ũ����ʩ��_____________(�ѧʽ)��
(2)С��ͬѧ����ͼ�ܽ���NaOH��������ѧ����(��NaOH�����������ܹ�������ѧ��Ӧ)��
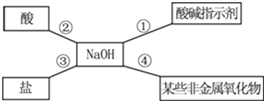
I��Ϊ����֤��Ӧ�٣�С�콫��ɫ��̪��Һ����NaOH��Һ�У���Һ����ɫ���_____��
II�����ݷ�Ӧ��˵��NaOH�����ܷⱣ�棬�����ڿ�����Ҫ���ʣ��仯ѧ��Ӧ����ʽΪ��__________________��
III��Ϊ����֤��Ӧ���ܹ���������ѡ���������_____��
a��Na2CO3�������� b��HCl�������� c��FeCl3 d��Ba(NO3)2
(3)�������һ��ʵ���ȥFeCl2��Һ��������CuCl2��д����Ҫ��������ͻ�ѧ����ʽ��ʵ����Ҫ�������裺_________��___________����ѧ����ʽ��___________��
���𰸡� Ca(OH)2 ��ɫ CO2+2NaOH=Na2CO3+H2O c �������Һ�м������������ ���� CuCl2+Fe=FeCl2+Cu
�����������⿼������ε����ʼ��������ʳ�ȥ�����л��е����������������Ҫȫ�棬����ע���ڳ���ʱ��Ҫ�����µ�������
��1���������������ԣ�һ�������ʯ�ң���ѧʽ����Ca(OH)2��
��2������ɫ��̪��Һ������ɫ����ɫ��̪��Һ����NaOH��Һ�У���Һ����ɫ��ɺ�ɫ��
���������Ʊ�������Ϊ��������������еĶ�����̼��Ӧ����̼���ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��CO2+2NaOH=Na2CO3+H2O��
�������������η�Ӧ���ڸ��ֽⷴӦ�����ֽⷴӦ��������������ˮ���������������ɡ�a��Na2CO3���������Ʋ���Ӧ������b��HCl���ᣬ�������Σ�����c��FeCl3��NaOH��Ӧ���������������������㸴�ֽⷴӦ����������ȷ��d��Ba��NO3��2���������ƻ��ʱ�������㸴�ֽⷴӦ�����������ܷ�Ӧ������ѡc��
��3����Ϊ�����û����Ȼ�ͭ�е�ͭ�������û���Ӧ�����Գ�ȥFeCl2��Һ��������CuCl2����ȡ��Һ���Թ��м���������ۡ�Ȼ����˵���������ͭ����Ӧ�Ļ�ѧ����ʽΪ��CuCl2+Fe=FeCl2+Cu��

 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д� ��ѧ�̸̳����¿α�ϵ�д�
��ѧ�̸̳����¿α�ϵ�д�����Ŀ��ij��ȤС���ͬѧΪ�ⶨijʯ��ʯ��̼���(���裺ʯ��ʯ�е����ʲ������ᷴӦ)��������������ȡһ��������ʯ��ʯ�����ձ��У���ijŨ�ȵ�ϡ����100g����5�μ��룬ÿ�γ�ַ�Ӧ��ȡ�����壬�����ˡ�ϴ�ӡ�����Ȳ�������أ�����ϡ����������ʣ�����������¼���£�
ʵ����� | ϡ���������(g) | ʣ����������(g) |
�� | 20 | 16.25 |
�� | 40 | 12.50 |
�� | 60 | m |
�� | 80 | 5.00 |
�� | 100 | n |

��ϸ�Ĺ۲�����ͼ�ش��������⣺
(1)��______��ʯ��ʯ�е�̼���������ǡ�÷�Ӧ��ϣ�
(2)������m= ______g��n=______g��
(3)�����ʯ��ʯ��Ʒ��ȫ��Ӧ���ɶ�����̼������Ϊ______��