题目内容
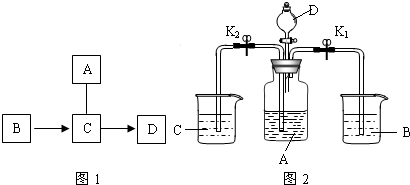
 A、B、C、D是实验室常见的四种物质,A、B、C在一定条件下的转化关系如图所示.在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,与A反应有CO2气体产生,与C发生中和反应,与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀.请回答:
A、B、C、D是实验室常见的四种物质,A、B、C在一定条件下的转化关系如图所示.在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,与A反应有CO2气体产生,与C发生中和反应,与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀.请回答:
(1)写出B、C的化学式:B______,C______.
(2)C转化成A的化学方程式为______.D与A反应的化学方程式为______,基本反应类型是______.
解:(1)在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.故C为氢氧化钙,化学式为Ca(OH)2;A为碳酸钙.A高温分解生成氧化钙和二氧化碳,B能与水反应生成氢氧化钙,所以B为氧化钙,化学式为CaO;
(2)C为氢氧化钙,A为碳酸钙,C转化成A可用氢氧化钙与二氧化碳反应,化学方程式为:CO2+Ca(OH)2═CaCO3↓+H20
D与A反应有CO2气体产生,与C发生中和反应,说明D是一种酸,D与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀,说明D是盐酸.所以D与A反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑此反应是由两种化合物相互交换成分生成另外两种化合物的反应,属于复分解反应.
故答案为:(1)CaO,Ca(OH)2.
(2)CO2+Ca(OH)2═CaCO3↓+H20. CaCO3+2HCl═CaCl2+H2O+CO2↑,复分解反应
分析:因为二氧化碳气体和氢氧化钠溶液反应生成碳酸钙白色沉淀,由此开始推断,可推出B为氧化钙,C为氢氧化钙,A为碳酸钙.C为碱,D能与C发生中和反应,确定D为酸,D能与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀,推断D为稀盐酸.
点评:此题主要是考查同学们的综合分析能力,不但要求同学们具备有关化合物的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.
(2)C为氢氧化钙,A为碳酸钙,C转化成A可用氢氧化钙与二氧化碳反应,化学方程式为:CO2+Ca(OH)2═CaCO3↓+H20
D与A反应有CO2气体产生,与C发生中和反应,说明D是一种酸,D与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀,说明D是盐酸.所以D与A反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑此反应是由两种化合物相互交换成分生成另外两种化合物的反应,属于复分解反应.
故答案为:(1)CaO,Ca(OH)2.
(2)CO2+Ca(OH)2═CaCO3↓+H20. CaCO3+2HCl═CaCl2+H2O+CO2↑,复分解反应
分析:因为二氧化碳气体和氢氧化钠溶液反应生成碳酸钙白色沉淀,由此开始推断,可推出B为氧化钙,C为氢氧化钙,A为碳酸钙.C为碱,D能与C发生中和反应,确定D为酸,D能与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀,推断D为稀盐酸.
点评:此题主要是考查同学们的综合分析能力,不但要求同学们具备有关化合物的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.

练习册系列答案
相关题目
 B.
B. C.
C. D.
D.
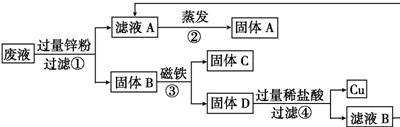
 (2012?太原)同学们在学习酸碱的化学性质时构建了如图知识网络,A、B、C、D是不同类别的无机化合物,“-”表示物质在一定条件下可以发生化学反应.请回答下列问题:
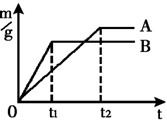
(2012?太原)同学们在学习酸碱的化学性质时构建了如图知识网络,A、B、C、D是不同类别的无机化合物,“-”表示物质在一定条件下可以发生化学反应.请回答下列问题: 如图为某课外小组为了验证可燃物燃烧条件,用白磷等为原料设计的四种实验A、B、C、D(实验前他们查找了白磷的着火点为40℃).
如图为某课外小组为了验证可燃物燃烧条件,用白磷等为原料设计的四种实验A、B、C、D(实验前他们查找了白磷的着火点为40℃).