题目内容
【题目】有A、B两种固体物质,A一种化肥,B广泛用作食品干燥剂.把A、B分别放入水中,前者所得溶液温度显著降低,后者与水反应生成C并放出大量的热;将A与C的粉末混合、研磨,会嗅到刺鼻的气味.
(1)A物质是_____,B物质是_____.
(2)指出C物质在农业生产中的一种用途_____.
(3)B与水反应的化学方程式是_____,此反应类型是_____反应.
【答案】硝酸铵 生石灰 改良酸性土壤 CaO+H2O═Ca(OH)2 化合
【解析】
根据A是一种化肥,B广泛用作食品干燥剂,把A、B分别放入水中,前者所得溶液温度显著降低,后者与水反应生成C并放出大量热,所以A是硝酸铵,其溶于水时吸热,B是氧化钙与水反应生成氢氧化钙,所以B是氧化钙,氢氧化钙和硝酸铵混合会生成刺激性气体氨气,氢氧化钙常用于改良酸性土壤或配制波尔多液,所以C是氢氧化钙。
(1)A是一种化肥,B广泛用作食品干燥剂,把A、B分别放入水中,前者所得溶液温度显著降低,后者与水反应生成C并放出大量热,所以A是硝酸铵,其溶于水时吸热,B是氧化钙与水反应生成氢氧化钙,所以B是氧化钙。
(2)氢氧化钙和硝酸铵混合会生成刺激性气体氨气,氢氧化钙常用于改良酸性土壤或配制波尔多液,所以C是氢氧化钙,可以用来改良酸性土壤。
(3)B与水的反应是氧化钙和水反应生成氢氧化钙,化学方程式是:![]() ,反应满足化合反应多变一的条件,属于化合反应。
,反应满足化合反应多变一的条件,属于化合反应。

 阅读快车系列答案
阅读快车系列答案【题目】实验室有一包固体药品,可能含有BaSO4、Na2CO3、CuSO4、NaCl、CaCl2、NaOH中的一种或几种,为确定其成分,某班同学在老师的指导下进行探究。
(一)定性探究:
Ⅰ.称取少量样品,加入足量水中充分溶解,过滤后得到白色沉淀和无色滤液。由实验现象可知,原固体中一定不含____;
Ⅱ.取Ⅰ中得到的滤液少量,设计实验继续探究原固体的成分,请帮他们完成实验报告并回答问题。
操作 | 现象 | 结论 |
向滤液中加入足量氯化钙溶液 | 产生白色沉淀 | 原固体中一定含有____ |
取上层清液,滴加____ | ____ | 原固体中不含NaOH |
其中,步骤加入足量氯化钙溶液的目的除了检验一定含有的物质外,还能起到的作用是____;
Ⅲ.再取Ⅰ中得到的滤液少量,进行如下操作:
![]()
同学们认为:原固体中一定含有NaCl。但是老师指出这个结论不正确,其理由是___(填序号)
A.滤液中含有Na2CO3,也能和AgNO3反应生成沉淀
B.滤液中的NaCl可能是由原固体中的Na2CO3和CaCl2反应生成
(二)定量探究:
在老师的指导下同学们又精确称量了10g原固体,进行如下实验:
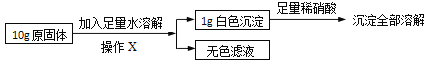
同学们认为,根据“沉淀全部溶解”的现象可确定白色沉淀的成分是____,则原固体中一定不含____;其中,操作X的名称是____,无色滤液中一定含有的阳离子是____。
试根据生成沉淀的质量计算原固体中氯化钙的质量分数,写出计算过程_____。
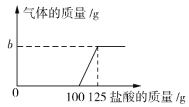
【题目】在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂。他们对该试剂进行了定量实验称取试剂19.8 g放入锥形瓶中,加入30.2 g的水,充分振荡,再向锥形瓶中依次滴加25 g盐酸充分反应。测得部分数据与图像如下。请根据有关信息回答问题。
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
加入盐酸的质量/g | 25 | 25 | 25 | 25 | 25 | 25 |
锥形瓶中物质的质量/g | 75 | 100 | a | 150 | 172.8 | 197.8 |
(1)a的数值为__________,兴趣小组的同学通过实验,得出该试剂已部分变质的结论,其依据是(通过实验数据和图像写出你的分析) _______________________________。
(2)b的数值为____________。
(3)计算该试剂中氢氧化钙的质量分数___________(写出计算过程,结果保留一位小数)。