��Ŀ����
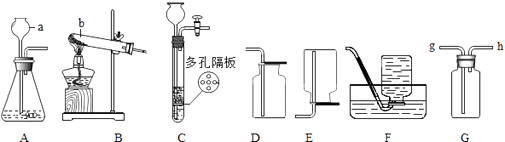
����Ŀ����ͼΪ���ֹ�����ܽ�����ߣ��ش��������⣺ 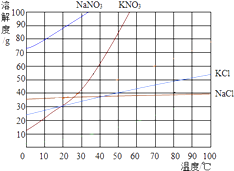
��1��NaCl���ܽ�����¶ȱ仯�Ĺ�������
��2����ʱKNO3��KCl���ܽ����ȣ�
��3��50��ʱ��KCl��Һ�����Ũ�ȣ���ʽ���ɣ�Ϊ��
��4��60��ʱ��10g NaCl��90g KNO3��ȫ�ܽ���100g����ˮ����ȴ��20���û�� �����С���û�С���NaCl��������gKNO3�ᾧ������
��5������һ���¶���һ��������NaCl��Һ��������Һ��������10gˮ��������1g���壬�ٺ�������5gˮ����������2g�˾��壬���¶Ȳ��䣬ԭ��Һ�պôﵽ������������ˮ��������g��
���𰸡�
��1�����¶ȵ����߶������仯����
��2��20
��3��![]()
��4��60
��5��7.5
���������⣺��1��NaCl���ܽ�����¶ȱ仯�Ĺ����ǣ� ������¶ȵ����߶������仯����2��20��ʱKNO3��KCl���ܽ����ȣ�
���20����3��50��ʱ��KCl���ܽ����40g����Һ�����Ũ��Ϊ�� ![]() ��
��
��� ![]() ����4��20��ʱ���Ȼ��Ƶ��ܽ�ȴ���35g������ص��ܽ����30g��60��ʱ���Ȼ��Ƶ��ܽ�ȴ���35g������ص��ܽ�ȴ���90g��10gNaCl��90gKNO3��ȫ�ܽ���100g����ˮ����ȴ��20���û��NaCl��������60gKNO3�ᾧ������
����4��20��ʱ���Ȼ��Ƶ��ܽ�ȴ���35g������ص��ܽ����30g��60��ʱ���Ȼ��Ƶ��ܽ�ȴ���35g������ص��ܽ�ȴ���90g��10gNaCl��90gKNO3��ȫ�ܽ���100g����ˮ����ȴ��20���û��NaCl��������60gKNO3�ᾧ������
���û�У�60����5��������Һ��������10gˮ��������1g���壬����˱�����Һ���ٺ�������5gˮ����������2g�˾��壬˵��5gˮ�ܽ�2g����ǡ�ñ��ͣ����1g�����ܽ���2.5gˮ��ǡ�ñ��ͣ���������¶Ȳ��䣬ԭ��Һ�պôﵽ������������ˮ��������10g��2.5g=7.5g��
���7.5��
�����㾫����������Ҫ�����˹����ܽ�����������õ����֪ʶ�㣬��Ҫ����1������ָ���¶�ʱ���ʵ��ܽ�ȣ��������ܽ���ж��ܽ��ԣ�2���Ƚ���ͬ�¶�ʱ����һ���¶ȷ�Χ�ڣ���ͬ�����ܽ�ȵĴ�С��3���ȽϺ�ȷ�����ʵ��ܽ�����¶�Ӱ��ij̶ȣ����ݴ�ȷ�����ʽᾧ����������ᴿ�ķ�����4��ȷ����Һ��״̬�������벻���ͣ�������ȷ�����⣮

 �߽�������ϵ�д�
�߽�������ϵ�д�����Ŀ������г���һЩ���������ڳ����µ� pH ��Χ�����гʼ��Ե��ǣ� ��
�������� | ������ | ţ�� | ������ | ����֭ |
pH ��Χ | 7.6��8.0 | 6.3��6.6 | 4.0��4.4 | 2.0��3.0 |
A.������
B.ţ��
C.������
D.����֭
����Ŀ���������ʵĻ�ѧʽ��д����������ȷ���ǣ� ��
ѡ�� | ���� | ��ѧʽ | ���� |
A | �Ҵ� | CH3CH2OH | �ƾ� |
B | ������ | CaO | ��ʯ�� |
C | ̼������ | Na2CO3 | �մ� |
D | �Ȼ��� | NaCl | ʳ�� |
A.A
B.B
C.C
D.D