题目内容
【题目】某化学兴趣小组为测定石灰石中主要成分碳酸钙的质量分数,取石灰石12.5g加入到盛有100g稀盐酸的烧杯中,恰好完全反应(假设杂质不溶于水也不与盐酸反应),产生4.4g气体.求:
(1)石灰石中碳酸钙的质量分数;
(2)反应后所得溶液中溶质的质量分数?(计算结果精确到0.1%)
【答案】
(1)解:设该石灰石样品中碳酸钙的质量为x,生成氯化钙的质量为y
CaCO3+2HCl═ | CaCl2+H2O+ | CO2↑ |
100 | 111 | 44 |
x | y | 4.4g |
![]()
x=10g
y=11.1g
石灰石中碳酸钙的质量分数为 ![]() ×100%=80%
×100%=80%
答:石灰石中碳酸钙的质量分数为80%
(2)解:反应后所得溶液中溶质的质量分数为 ![]() ×100%=10.5%
×100%=10.5%
【解析】解:(1)设该石灰石样品中碳酸钙的质量为x,生成氯化钙的质量为y
CaCO3+2HCl═ | CaCl2+H2O+ | CO2↑ |
100 | 111 | 44 |
x | y | 4.4g |
![]()
x=10g
y=11.1g
石灰石中碳酸钙的质量分数为 ![]() ×100%=80%;(2)明确总溶液的质量是10g+100g-4.4g,则反应后所得溶液中溶质的质量分数为
×100%=80%;(2)明确总溶液的质量是10g+100g-4.4g,则反应后所得溶液中溶质的质量分数为 ![]() ×100%=10.5%。
×100%=10.5%。
【考点精析】认真审题,首先需要了解根据化学反应方程式的计算(各物质间质量比=系数×相对分子质量之比).

【题目】兴趣小组的同学发现,利用如图装置,可完成许多实验,请你回答下列问题: 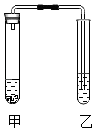
(1)【实验】
1 | 2 | 3 | |
甲(药品) | 浓氨水 | 碳酸钠、稀盐酸 | 水、氢氧化钠固体 |
乙(药品) | 无色酚酞溶液 | 澄清石灰水 | 水 |
现象 | 乙导管口有气泡冒出, | 乙导管口有气泡冒出 | |
结论和解释 | 分子具有的一条性质是 | 写出其中的一个化学方程式: | 出现该现象的原因是 |
(2)【交流与评价】 ①实验3中将氢氧化钠固体换成 , 原理一样,也会出现相同的现象.
②反应停止后将实验2中甲、乙两试管废液倒在一起,产生更多的沉淀,则反应停止后实验2甲试管溶液中的溶质是、 .
【题目】如图所示的暖宝宝是一种防寒用品.小明想知道暖宝宝中的主要成分有哪些?暖宝宝发热的原因是什么? 
(1)小明探究:暖宝宝中的主要成分是什么? 剪开内包装袋,倒出其中的粉末,发现呈黑色.
【提出猜想】该黑色粉末可能含有木炭粉、铁粉、氧化铜
中的一种或几种.
【初步验证】将磁铁靠近黑色粉末,部分被吸引.
【得出结论】该黑色粉末中一定含有 , 可能含有 .
【查阅资料】木炭与稀硫酸不反应,氧化铜与稀硫酸反应能产生蓝色溶液.
【进行实验】
实验编号 | 实验操作 | 实验现象 |
① | 取少量黑色粉末于试管中,加足量稀硫酸 | 固体部分溶解,有气泡产生,溶液未变 |
② | 取实验①的残渣灼烧,将内壁涂有澄清石灰水的小烧杯罩在上方 | 澄清石灰水变浑浊 |
由实验①可知,该黑色粉末中一定含有 , 一定不含 .
写出实验①的化学反应方程式 .
由实验②可知,该黑色粉末中一定含有 .
(2)小明思考:暖宝宝为什么会发热? 【查阅资料】暖宝宝中除含有铁粉、木炭外,还含有食盐和水.
①暖宝宝贴在衣服上与空气接触后会发热的原因是 . 由此可见,人们可以利用化学反应放出的热量来造福人类,请你再举一例: .
②请你猜测暖宝宝中氯化钠的作用是 .
【题目】太湖水经苏州胥江水厂处理的大致流程如下. 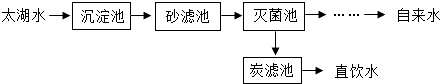
(1)从沉淀池中出来的水经过沙滤池的操作称为: . 经沙滤池后的水在灭菌池中被通入的臭氧(O3)进行杀菌处理,再经一系列后续处理成为自来水进入千家万户;在深度处理区,炭滤池中活性炭的作用是:
(2)有人做了如下的甲、乙2个实验.因在乙实验中得到一些有色沉淀,于是就说“自来水没有纯水好”.某校兴趣小组同学为验证上述说法的真伪,又增做了丙和丁2个对比试验(均在室温下) 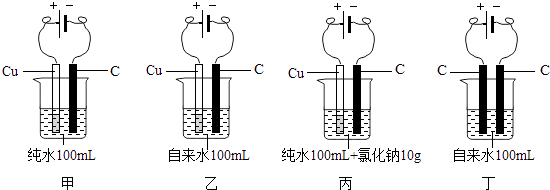
项目 | 甲 | 乙 | 丙 | 丁 |
与电源正极相连的电极附近区域 | 现象不明显 | 有小气泡产生,渐有有色沉淀生成,沉淀颜色逐渐加深 | 有刺激性气味的较多气泡产生,且有许多有色沉淀生成 | 有小气泡产生 |
与电源负极相连的电极附近区域 | 现象不明显 | 有小气泡产生 | 有较多气泡产生 | 有小气泡产生,渐有少量沉淀生成 |
①上述实验中能量转换的形式为: .
②由上述4个对比试验可知:装置(填序号)中水样的导电能力最强.在上述对比试验中,生成有色沉淀的主要原因是:
(3)水厂的检测人员用浑浊度仪测出该厂自来水中颗粒物的量为0.55;用pH仪测出水质的度为7.66,此时水质呈弱性.这是因为自来水中含有了多种天然水溶解的对人体有益的微量元素的缘故.且在合格标准内.