题目内容
【题目】将44.4克碱式碳酸铜粉末加热一段时间,经测定铜元素的质量占试管内的80℅.试求(1)求此时试管中氧化铜的质量?(2)若将试管内的剩余固体全部溶于100克盐酸溶液,求所得溶液中溶质的质量分数
【答案】(1)32g (2)40.9%
【解析】根据铜元素质量守恒计算出固体剩余物的质量,与原固体的质量之差即为产生的气体(二氧化碳和水)的质量,由此可根据化学方程式计算试管中氧化铜的质量等。44.4克碱式碳酸铜中铜元素的质量=44.4克×128/222=25.6克,当其质量占试管内的80℅时,固体剩余物的质量=25.6克/80%=32克。则产生的气体的质量=44.4克-32克=12.4克。设此时试管中氧化铜的质量为x。
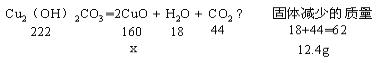
x=32g
说明此时试管中的固体都是氧化铜。将其全部溶于100克盐酸溶液中设所得溶液中溶质的质量为y。
CuO +2HCl =CuCl2 +H2O
80 135
32g y
y=54g
所以所得溶液中溶质的质量分数=54g/(32g+100g)×100%=40.9%

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目