题目内容
(2007?宿迁)利用海水可以制备金属单质,其流程如下图所示:
(1)实验室将粗盐制成精盐的过程中,常采用操作把不溶性杂质除去.
(2)步骤③中涉及的化学反应方程式为.
(3)通过以下步骤可以制取金属Y

步骤④中涉及的化学反应方程式为;该反应的类型为.
【答案】分析:(1)过滤可以把不溶性物质分离出来.
(2)氢氧化镁和盐酸可以发生中和反应,根据方程式书写规则进行书写.
(3)根据图示信息可知氯化镁通电生成了金属单质和气体单质,是镁和氧气.书写时要注意条件和符号.
解答:解:(1)通常将不溶性物质从溶液中除去的方法是溶解、过滤.
(2)氢氧化镁是碱和盐酸发生中和反应生成氯化镁和水,配平后方程式为:Mg(OH)2+2HCl═MgCl2+2H2O
(3)根据图示知氯化镁通电生成了金属单质镁和气体单质氧气,条件是通电,方程式为MgCl2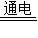 Mg+Cl2↑,反应是由一种物质生成两种物质,符合分解反应的定义.
Mg+Cl2↑,反应是由一种物质生成两种物质,符合分解反应的定义.
故答案为:(1)过滤;
(2)Mg(OH)2+2HCl═MgCl2+2H2O;
(3)MgCl2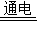 Mg+Cl2↑;分解反应.
Mg+Cl2↑;分解反应.
点评:本题主要以海水资源的利用为载体考查了学生对化学方程式的书写技巧和反应类型的判断能力.
(2)氢氧化镁和盐酸可以发生中和反应,根据方程式书写规则进行书写.
(3)根据图示信息可知氯化镁通电生成了金属单质和气体单质,是镁和氧气.书写时要注意条件和符号.
解答:解:(1)通常将不溶性物质从溶液中除去的方法是溶解、过滤.
(2)氢氧化镁是碱和盐酸发生中和反应生成氯化镁和水,配平后方程式为:Mg(OH)2+2HCl═MgCl2+2H2O
(3)根据图示知氯化镁通电生成了金属单质镁和气体单质氧气,条件是通电,方程式为MgCl2
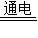 Mg+Cl2↑,反应是由一种物质生成两种物质,符合分解反应的定义.
Mg+Cl2↑,反应是由一种物质生成两种物质,符合分解反应的定义.故答案为:(1)过滤;
(2)Mg(OH)2+2HCl═MgCl2+2H2O;
(3)MgCl2
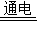 Mg+Cl2↑;分解反应.
Mg+Cl2↑;分解反应.点评:本题主要以海水资源的利用为载体考查了学生对化学方程式的书写技巧和反应类型的判断能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目