题目内容
某化学兴趣小组根据下列转化关系在实验室中模拟炼铁,并对产物成分进行探究。
(1)炼铁的原理是 (用化学方程式表示)。
(2)经初步分析得知,无色气体A不含有单质,黑色粉末B的成分是一种或两种单质。上述转化关系中,生成一氧化碳的化学方程式是 。
(3)甲、乙两个兴趣小组分别对无色气体A和黑色粉末B的成分进行探究。
【猜想与假设】
甲组在分析了炼铁的原理后,认为无色气体A中可能有CO2,也可能有未反应的 。
乙组认为黑色粉末的成分中存在以下两种情况:
假设一:只含有铁。假设二:含有 。
【实验探究】
为验证甲组的猜想,同学们按下图所示装置进行实验(箭头表示气体流向)。
Ⅰ澄清石灰水 Ⅱ浓硫酸 Ⅲ氧化铜粉末
上述实验装置Ⅱ中浓硫酸的作用是吸收水蒸气,装置Ⅰ的作用是 ,装置Ⅲ的作用是 。当看到Ⅰ中澄清石灰水变浑浊,Ⅲ中黑色固体变成红色后,可以确定无色气体A的成分是 。
为验证乙组中假设二是否成立,请你设计实验用物理和化学两种方法完成以下探究。
| 实验方法 | 实验操作 | 实验现象 | 实验结论 |
| 物理方法 | | | 假设二成立 |
| 化学方法 | | | 假设二成立 |
【交流反思】针对甲组实验存在的缺陷,同学们一起进行了改进,解决了污染环境问题。
(1)3CO + Fe2O3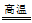 2Fe + 3CO2 (2)2C + O2
2Fe + 3CO2 (2)2C + O2 2CO
2CO
(3)【猜想与假设】CO 假设二:铁和碳
【实验探究】①检验CO2 检验CO CO2和CO
②注:以下实验方法中,每个操作和现象都正确得1分。实验方法 实验操作 实验现象 物理方法 取少量黑色粉末B,用磁铁吸引 部分黑色粉末被吸引上来 化学方法 取少量黑色粉末B于试管中,加入过量的稀盐酸 部分黑色粉末溶解,产生无色气泡
解析试题分析:(1)炼铁是利用一氧化碳还原氧化铁:3CO + Fe2O3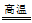 2Fe + 3CO2
2Fe + 3CO2
(2)无色气体A不含有单质,即不含氧气,可能是一氧化碳和二氧化碳的混合气体,黑色粉末B的成分是一种或两种单质,即可能是铁或铁和碳的混合物;实验室要得到还原性气体一氧化碳可利用碳和氧气反应得到;
(3)一氧化碳还原氧化铁会生成二氧化碳,由于一氧化碳可能没有完全反应,气体中也可能含有一氧化碳;由于反应物中含有碳,故黑色粉末可能是铁或铁和碳的混合物;
①甲组实验是要证明二氧化碳和一氧化碳的存在,可用澄清石灰水检验二氧化碳,利用一氧化碳的的还原性检验二氧化碳。
②假设二成立说明是铁和碳的混合物,用磁铁吸引后只有部分黑色物质能吸引上来;若用化学方法,则可利用铁能酸反应的性质,可看见部分粉末溶解。
考点:炼铁的原理、物质的检验

 名校课堂系列答案
名校课堂系列答案在化学课上,甲同学将燃烧的钠(Na)迅速伸入到盛有CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质.老师告诉同学们,这种黑色颗粒和白色物质都是化学实验室中的常用药品之一。
【提出问题】黑色颗粒和白色物质分别是什么?
【进行猜想】甲认为黑色颗粒是 炭(C),白色物质可能是碳酸钠( Na2CO3)或氧化钠(Na2O),乙同学还认为白色物质是氢氧化钠(NaOH).经过分析甲同学认为乙同学的猜想是错误的,其理由是_______________________,
【查阅资料】氧化钠为白色粉末,溶于水生成氢氧化钠,氢氧化钠与盐酸反应生成氯化钠和水。碳酸钠也是白色粉末,与盐酸反应会产生二氧化碳、水、氯化钠。
【实验探究】甲同学对黑色颗粒,白色物质分别是什么物质进行实验探究.
| 实验步骤 | 实验操作 | 实验现象 | 结论 |
| 步骤1 | 在氧气流中充分燃烧黑色固体,并把产生的气体通入澄清石灰水中 | 黑色固体完全消失,澄清石灰水变浑浊 | 黑色固体是____________ |
| 步骤2 | 取少量白色固体于试管中,加入适量水,振荡,样品全部溶于水,向其中加入盐酸 | 产生气泡 | 白色固体是___________ |
【拓展反思】通过这个实验,你对燃烧条件有什么新的认识?_______________________________________________
同学们为了研究氧化铁能否在氯酸钾制取氧气的实验中起催化作用,进行了以下实验:
【资料】①氯酸钾分解反应的化学方程式为 2KClO3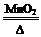 2KCl+3O2↑。
2KCl+3O2↑。
②氯酸钾和氯化钾均能溶于水。
【实验一】氧化铁能否在氯酸钾制取氧气实验中加快反应速率。
| 实验编号 | KClO3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
| 1 | 0.6 | | 67 | 1800 |
| 2 | 0.6 | 0.2g二氧化锰 | 67 | 36.5 |
| 3 | 0.6 | g 氧化铁 | 67 | 89.5 |
(1)实验3中氧化铁的质量为 。
(2)以上实验采用了 的实验方法。
(3)实验一得到的结论是 。
【实验二】为证明氧化铁是该反应的催化剂,同学们又完成了以下的实验:
Ⅰ.在实验3反应后的混合物中加足量的水溶解,过滤得到红色固体,洗涤干燥并用电子天平称量,质量为0.2g。
Ⅱ.将一定量的CO通入滤出的固体,按下图进行实验:

甲同学的实验报告如下:
| 装置 | 实验现象 | 实验分析 |
| A | 红色固体全部变黑 | 生成了铁 |
| B | 石灰水变浑浊 | 产生二氧化碳 |
(4)写出A中玻璃管内发生反应的化学方程式 。
【实验结论】氧化铁能在氯酸钾制取氧气反应中起催化剂。
【实验反思】乙同学查阅资料发现一氧化碳还原氧化铁后剩余固体可能由氧化亚铁、四氧化三铁、铁粉和未反应的氧化铁中的一种或几种组成。
为了研究剩余固体的成分,丙同学查阅了以下资料:
| | 铁粉 | 氧化亚铁 | 氧化铁 | 四氧化三铁 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 磁性 | 有 | 无 | 无 | 有 |
| 与CO反应 | 不反应 | 反应 | 反应 | 反应 |
| 与稀盐酸反应 | 反应 | 生成氯化亚铁和水 | 生成氯化铁和水 | 生成氯化亚铁、氯化铁和水 |
| 与硫酸铜溶液反应 | 反应 | 不反应 | 不反应 | 不反应 |
(5)丙同学认为剩余固体中一定没有氧化铁,原因是____________。
(6)测定剩余固体的组成。
| 步骤 | 实验操作 | 实验现象 | 结论和解释 |
| 1 | 用磁铁吸引剩余固体 | _____________ | 剩余固体中没有氧化亚铁。 |
| 2 | __________________ | ______________ | 剩余固体中只有铁粉。 |
根据下图实验,回答以下问题。 

(1)写出A装置中反应的化学方程式_______。
(2)将用石蕊溶液染成紫色的干燥纸花,放入集气瓶B中,观察到的现象是_______。
(3)写出C装置中反应的化学方程式_______,其中水的作用为_______。
(4)河水经过D装置后得到的水是_______(填“纯净物”或“混合物”)。
(5)下列叙述中不正确的是_______。
| A.水体污染会危害人体健康 |
| B.生活中养成良好的用水习惯 |
| C.工业废水经过处理达标后再排放 |
| D.禁止使用农药、化肥,以免造成水体污染 |
学校实验室的废液缸中收集了学生在实验室制取CO2后残留的废液.小红同学想探究废液中溶质的成分,请你一同探究并回答下列问题:
【提出问题】废液中的溶质是什么物质?
【做出猜想】小红认为废液中的溶质只有CaCl2.你认为还可能含有的溶质是 .(化学式)
【查阅资料】CaCl2溶质呈中性.
【实验与结论】为了验证小红的结论,小红进行了下面是的实验:
| 实验操作 | 实验现象 | 结论 |
| 取少量废液于试管中,向其中滴加几滴无色酚酞溶液 | 溶液呈 . | 废液中只有 ,自己的猜想正确 |
(1)你认为小红的实验 (填“能”或“不能”)证明她的猜想,理由是 .
(2)如果想要证明我的猜想是正确的,请补充完下面的实验方案
| 实验操作 | 实验现象 |
| ①取少量废液与试管中,向其中加入石蕊溶液 | 废液变为 |
| ②取少量废液与试管中,向其中加入 . | 有气体产生 |
| ③取少量废液与试管中,向其中加入 . |
(3)若实验证明你的猜想是正确的,想要处理废液只得到CaCl2溶液,应向废液中加入过量的 ,反应完成过 .


 CO↑+CO2↑+H2O
CO↑+CO2↑+H2O