题目内容
下列装置用于实验室里CO2的制备、净化.分析回问题.
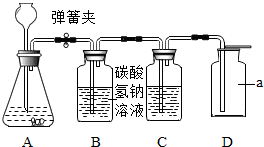
(1)仪器a的名称是 ;
(2)分析三组药品:①碳酸钠粉末和稀盐酸 ②块状石灰石和稀硫酸 ③块状石灰石和稀盐酸,选择一组药品制取CO2,其反应可用化学方程式表示为 ;
(3)试验时,C中盛有的是 ;能用D装置收集CO2的原因是 ;
(4)反应结束时将弹簧夹关闭,在A中看到的现象是 .

(1)仪器a的名称是
(2)分析三组药品:①碳酸钠粉末和稀盐酸 ②块状石灰石和稀硫酸 ③块状石灰石和稀盐酸,选择一组药品制取CO2,其反应可用化学方程式表示为
(3)试验时,C中盛有的是
(4)反应结束时将弹簧夹关闭,在A中看到的现象是
考点:二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)从仪器的图形和用途去分析;
(2)从①碳酸钠粉末和稀盐酸反应速度太快,②块状石灰石和稀硫酸反应生成的硫酸钙微溶于水 ③块状石灰石和稀盐酸,反应速率适中,去分析;
(3)从B装置可除去氯化氢气体,所以C装置可放浓硫酸(具有吸水性)除去水分;由于二氧化碳的密度比空气大,去分析;
(4)从反应结束时将弹簧夹关闭,由于石灰石和稀盐酸没有分开,继续反应生成二氧化碳,会使锥形瓶内气体增多压强增大,锥形瓶内的水被压入长颈漏斗中去分析.
(2)从①碳酸钠粉末和稀盐酸反应速度太快,②块状石灰石和稀硫酸反应生成的硫酸钙微溶于水 ③块状石灰石和稀盐酸,反应速率适中,去分析;
(3)从B装置可除去氯化氢气体,所以C装置可放浓硫酸(具有吸水性)除去水分;由于二氧化碳的密度比空气大,去分析;
(4)从反应结束时将弹簧夹关闭,由于石灰石和稀盐酸没有分开,继续反应生成二氧化碳,会使锥形瓶内气体增多压强增大,锥形瓶内的水被压入长颈漏斗中去分析.
解答:解:(1)由仪器的图形和用途可知a为集气瓶;故答案为:集气瓶;
(2):①碳酸钠粉末和稀盐酸反应速度太快,生成的二氧化碳不易收集,所以不选; ②块状石灰石和稀硫酸反应生成的硫酸钙微溶于水,覆盖在碳酸钙的表面,阻止碳酸钙与稀硫酸接触,使反应停止; ③块状石灰石和稀盐酸,反应速率适中,可用来制取二氧化碳;石灰石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳.其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)由于制取的二氧化碳中含有一定的水分和氯化氢气体,B装置可除去氯化氢气体,所以C装置可放浓硫酸(具有吸水性)除去水分;由于二氧化碳的密度比空气大,所以可用向上排空气法收集;
故答案为:浓硫酸 二氧化碳的密度比空气大;
(4)反应结束时将弹簧夹关闭,由于石灰石和稀盐酸没有分开,继续反应生成二氧化碳,会使锥形瓶内气体增多压强增大,锥形瓶内的水被压入长颈漏斗中;故答案为:长颈漏斗内液面上升.
(2):①碳酸钠粉末和稀盐酸反应速度太快,生成的二氧化碳不易收集,所以不选; ②块状石灰石和稀硫酸反应生成的硫酸钙微溶于水,覆盖在碳酸钙的表面,阻止碳酸钙与稀硫酸接触,使反应停止; ③块状石灰石和稀盐酸,反应速率适中,可用来制取二氧化碳;石灰石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳.其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)由于制取的二氧化碳中含有一定的水分和氯化氢气体,B装置可除去氯化氢气体,所以C装置可放浓硫酸(具有吸水性)除去水分;由于二氧化碳的密度比空气大,所以可用向上排空气法收集;
故答案为:浓硫酸 二氧化碳的密度比空气大;
(4)反应结束时将弹簧夹关闭,由于石灰石和稀盐酸没有分开,继续反应生成二氧化碳,会使锥形瓶内气体增多压强增大,锥形瓶内的水被压入长颈漏斗中;故答案为:长颈漏斗内液面上升.
点评:本题综合考查了实验室里CO2的制备原理、净化.等问题、是基础,要熟记.

练习册系列答案
相关题目
只用一种试剂区别NaNO3、AgNO3、Na2CO3三种无色溶液,可选用( )
| A、CaCl2溶液 |
| B、盐酸 |
| C、稀硝酸 |
| D、氯化钠溶液 |
下列物质间的转化不能一步实现的是( )
| A、NaHCO3-CO2 |
| B、CO2-CaCO3 |
| C、CaO-Cacl2 |
| D、KNO3-K2CO3 |
 如图所示,完成下列问题
如图所示,完成下列问题