题目内容
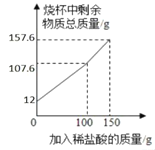
【题目】为了测定石灰石中碳酸钙的含量,小乐进行了如下实验:取12g石灰石放于烧杯中,向烧杯中滴加150g稀盐酸,产生气体质量与加入稀盐酸的质量之间的关系如图所示。整个过程不考虑稀盐酸的挥发和气体的溶解,石灰石中的杂质也不与稀盐酸反应。求:
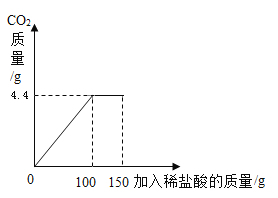
(1)产生CO2的总质量为_____g
(2)石灰石中碳酸钙的质量分数_____(写出计算过程,最后结果精确至0.1%)。
(3)请画出烧杯中剩余物质总质量(纵坐标)随加入盐酸质量(横坐标)的关系图_____。
【答案】4.4g 83.3% 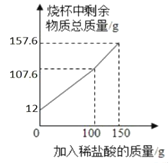
【解析】
碳酸钙和稀盐酸反应生成氯化钙和二氧化碳和水,随着盐酸量的增加,二氧化碳的质量逐渐增加,直到碳酸钙反应完全,二氧化碳质量不再增加。
根据图可知,生成的二氧化碳的质量为4.4g。
设石灰石中碳酸钙的质量分数为x
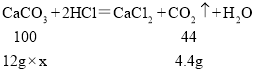
![]()
x≈83.3%
加入盐酸前,固体为12g,所以起点为12g,加入100g盐酸时恰好完全反应。所以此时对应的质量为107.6g,继续加入50g稀盐酸,总质量也增加50g,所以为157.6g。

练习册系列答案
 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目