题目内容
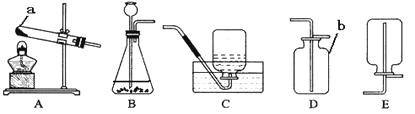
【题目】I.下列是研究燃烧的条件及氧气、水、二氧化碳的实验。根据图示,回答问题。
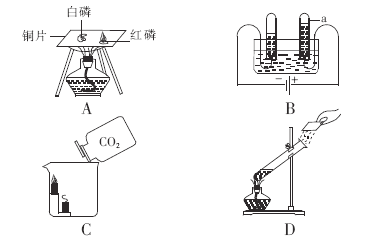
(1)A中先燃烧的是白磷,结论是________。
(2)B中反应的化学方程式为_________。
(3)C实验可以得出二氧化碳化学性质是______。
(4)通过D中的实验操作后收蒸馏水,滴入肥皂水的现象为_____,产生水蒸气
现象的微观解释是_________。
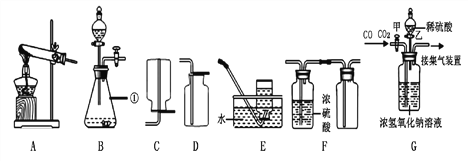
Ⅱ.根据下图实验回答问题。
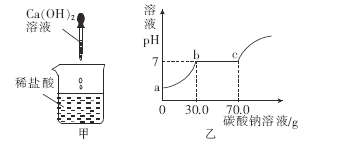
取甲反应后的溶液,滴加Na2 CO3溶液,溶液pH的变化如图乙所示,则c点的含义是_______,与CaCl2反应的碳酸钠溶液的质量为_______g。
【答案】 燃烧须达到可燃物的着火点 2H2O![]() 2H2↑+ O2 ↑ 既不燃烧也不支持燃烧的性质 泡沫多、浮渣少 水分子加热,分子间隔变大,冷却分子间隔变小 所加的碳酸钠与盐酸恰好反应,溶液呈中性 40
2H2↑+ O2 ↑ 既不燃烧也不支持燃烧的性质 泡沫多、浮渣少 水分子加热,分子间隔变大,冷却分子间隔变小 所加的碳酸钠与盐酸恰好反应,溶液呈中性 40
【解析】(1)A中白磷先燃烧,说明燃烧须达到可燃物的着火点;
(2)B中是水在通电的条件下反应生成氢气和氧气,反应方程式为 : 2H2O 通电 2H2↑+ O2↑;
(3)二氧化碳倒入烧杯中蜡烛熄灭,说明二氧化碳既不燃烧也不支持燃烧;
(4)D操作收集到的水是蒸馏水,是软水,当滴入肥皂水后泡沫多、浮渣少;水蒸发产生水蒸气的原因是水加热后水分子之间的间隙变大,冷却后水分子之间的间隙又变小;
(5)c点表示所加的碳酸钠与盐酸恰好反应,溶液呈中性;b—c段碳酸钠与氯化钙反应,故反应的碳酸钠溶液的质量为70.0g-30.0g=40.0g;

 名校课堂系列答案
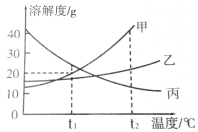
名校课堂系列答案【题目】下列实验符合下图所示变化趋势的是( )
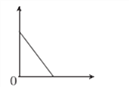
选项 | 实验 | 横坐标 | 纵坐标 |
A | 向一定量氢氧化钠 溶液中滴加稀硫酸 | 稀硫酸的质量 | 水的质量 |
B | 加热一定量氯酸钾固体 | 反应时间 | 剩余固体中 氧元素的质量 |
C | 向一定量饱和硝酸钾溶液中加水 | 加水的质量 | 溶质的质量分数 |
D | 向一定量镁粉中加入稀盐酸 | 稀盐酸的质量 | 镁元素的质量 |
A. A B. B C. C D. D
【题目】某同学用一定质量分数的Na2C03溶液做“Na2CO3与CaCl2反应”的实验。其五次实验结
果如下表所示:
实验次数 | 氯化钙的质量/g | 碳酸钠溶液的质量/g | 碳酸钙的质量/g |
1 | 1.11 | 80 | 1 |
2 | 2.22 | 80 | 2 |
3 | 4.44 | 80 | 4 |
4 | 6.66 | 100 | 5 |
5 | 11.1 | 160 | X |
根据实验结果回答下列问题:
(1)哪几次反应碳酸钠有剩余__(填序号)。
(2)表中X的值是_______。
(3)试计算碳酸钠溶液中溶质的质量分数_________。
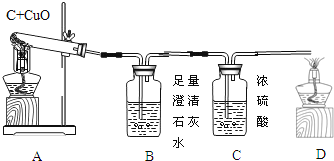
【题目】如图A为碳还原氧化铜的实验装置图。老师指出反应物不同的质量比可能会影响生成物的种类,在学习时,可以从定性观察和定量分析两个角度来判断生成物。请你跟随老师的思路,探究碳还原氧化铜生成的气体.(浓硫酸具有吸水性)
【提出问题】:碳还原氧化铜生成的气体是什么?
【作出猜想】:猜想①:CO 猜想②:CO2猜想③:__________
【实验设计】:装置图如图:
方案一:从定性观察角度判断:
(1)若猜想3成立
Ⅰ、B处的现象是___________________
Ⅱ、D处发生反应的化学反应方程式___________________________
方案二:从定量计算角度判断:
测定表格中的四个数据:
反应前的质量 | 反应后的质量 | |
装置A | m1 | m2 |
装置B | m3 | m4 |
Ⅰ、若猜想②成立,则m4m3___m1m2(选填“>”、“<”或“=”),此时A中的现象是__________________,B发生反应的化学方程式为 _________________________
Ⅱ、实际测量中B增加的质量小于理论值,请你分析可能的原因__________________________