题目内容
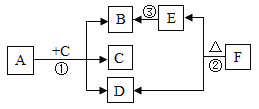
【题目】如图表示几种物质之间的转化关系,“→”表示一种物质通过化学反应可生成另一种物质“反应的条件、其他反应物或生成物已经略去”,请回答问题:
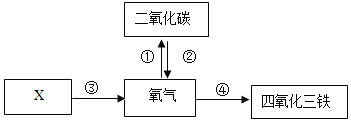
(1)转化①的另一种反应物的化学式可能是_____;
(2)转化②利于维持空气中氧气含量的基本稳定,绿色植物实现转化②的过程发生了_____(填标号)
A 呼吸作用 B 光合作用 C 燃烧反应
(3)若转化③是分解反应,从组成上分析,X中一定含有_____元素。
(4)转化④反应的文字表达式_____,则可以表明该变化是化学变化的实验现象是_____。
【答案】碳、一氧化碳、甲烷、酒精等 B 氧 ![]() 生成黑色固体
生成黑色固体
【解析】
二氧化碳和碳高温生成一氧化碳,一氧化碳和氧气点燃生成二氧化碳,铁在氧气中点燃生成四氧化三铁,绿色植物通过光合作用把二氧化碳和水合成有机物葡萄糖,同时生成氧气。
(1)转化①的另一种反应物的化学式可能是碳、一氧化碳、甲烷、酒精等,这是因为这些物质燃烧都能够生成二氧化碳。
(2)转化②利于维持空气中氧气含量的基本稳定,绿色植物通过光合作用把二氧化碳和水合成有机物葡萄糖,同时生成氧气,故选B。
(3)若转化③是分解反应,从组成上分析,X中一定含有氧元素。
(4)转化④中,铁在氧气中点燃生成四氧化三铁,反应的文字表达式为![]() ,化学变化是有新物质生成的变化,则可以表明该变化是化学变化的实验现象是生成黑色固体。
,化学变化是有新物质生成的变化,则可以表明该变化是化学变化的实验现象是生成黑色固体。

 名校课堂系列答案
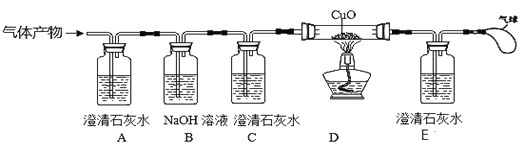
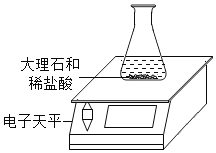
名校课堂系列答案【题目】某同学对“影响稀盐酸和大理石反应快慢的因素”进行探究.选取的药品:成分相同的粉末状大理石、块状大理石两种样品;浓度为16%、9%的稀盐酸.采用控制变量法设计实验方案,以5分钟内收集到CO2的质量作为判断依据.已知稀盐酸足量且样品中杂质不与稀盐酸反应,实验装置如图.读取电子天平的示数,据此计算生成的CO2的质量,记录的数据如表
实验序号 | 大理石 (各6g) | 稀盐酸的浓度 | 反应开始到5分钟产生CO2的质量 | 反应结束产生的CO2的质量 |
① | 块状 | 16% | 2.16g | 2.2g |
② | 块状 | 9% | 1.42g | 2.2g |
③ | 粉末 | 16% | 2.33g | 2.2g |
④ | 粉末 | 9% | 1.93g | m2 |
(1)稀盐酸的浓度对该反应快慢的影响:_____.
(2)实验过程中,通过观察如图装置中的哪一现象可判断反应结束_____.
(3)结合表格分析,实验④反应结束后m2的值_____.
(4)探究大理石的颗粒大小对该反应快慢的影响,其实验序号分别是_____.
(5)计算该大理石(6g)样品中含碳酸钙的质量为_____.
【题目】“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;
b.可能与锌的形状有关。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验 编号 | 硫酸的质量 分数(均取 20 mL) | 锌的形状 (均取1 g) | 氢气的体积(mL) (均收集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 30% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式:________________________。
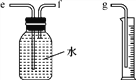
(2)小兵用如图所示装置收集并测量氢气的体积,其中量筒的作用是________________________________________,氢气应从________(填“e”“f”或“g”)管通入。
【收集证据】(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________。
【得出结论】(4)结论是________________________________________________________________。
(5)下表是小兵第①组实验的详细数据。
时段(均 为1分钟) | 第1 分钟 | 第2 分钟 | 第3 分钟 | 第4 分钟 | 第5 分钟 | 第6 分钟 |
H2的体积 | 3.1 mL | 16.7 mL | 11.9 mL | 9.6 mL | 7.6 mL | 6.0 mL |
请描述锌与硫酸反应的快慢的变化并解释原因:______________________________。
(6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。___________________。