题目内容
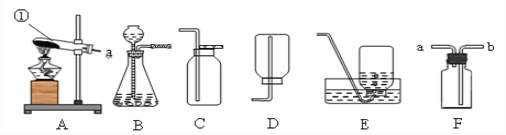
【题目】实验室常用下列装置制取气体,请你根据所学知识回答下列问题。
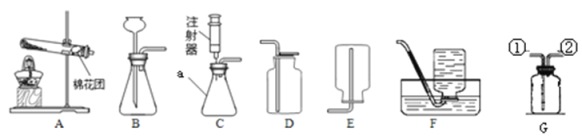
(1)写出标号仪器的名称:a ___________________
(2)若实验室用加热高锰酸钾的方法制取比较纯净的氧气,应选用的装置组合是__________反应的化学方程式是____________________________,基本反应类型是 ____________,集满氧气的集气瓶应____(填“正”或“倒”)放在桌面上,原因是 ___________________________
(3)若装置G用排空气法收集氧气,则气体应从________(填“①”或“②”)端通入,若要检验该装置已经集满氧气的方法是______________________________。
(4)实验室在常温下用块状电石(化学式为CaC2)和水反应制取难溶于水、密度比空气小的乙炔气体(又名电石气,化学式为C2H2),同时生成另一种物质——氢氧化钙。写出该反应的化学方程式___________________________,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂。你认为上图(A~F)中最适合制取较干燥的乙炔气体的装置组合是____。
(5)装置的气密性是保证气体实验成功的关键,下列图示操作中,不能用于检查气密性的是____

【答案】锥形瓶 AF 2KMnO4![]() K2MnO4+MnO2+O2↑ 分解反应 正 氧气的密度比空气大 ① 把带火星的木条放到②导气管口,复燃即满 CaC2+2H2O==Ca(OH)2+C2H2↑ CE A
K2MnO4+MnO2+O2↑ 分解反应 正 氧气的密度比空气大 ① 把带火星的木条放到②导气管口,复燃即满 CaC2+2H2O==Ca(OH)2+C2H2↑ CE A
【解析】
(1)仪器a的名称为锥形瓶;
(2)高锰酸钾制取氧气需要进行加热,故发生装置选A,氧气密度大于空气,制取干燥的氧气可用向上排空气法进行收集,故收集装置选F,故装置组合为AF;反应的化学方程式是2KMnO4![]() K2MnO4+MnO2+O2↑;该反应符合一变多的特征,属于分解反应;集满氧气的集气瓶应正放在桌面上,原因是氧气的密度大于空气,防止氧气逸散;
K2MnO4+MnO2+O2↑;该反应符合一变多的特征,属于分解反应;集满氧气的集气瓶应正放在桌面上,原因是氧气的密度大于空气,防止氧气逸散;
(3)氧气密度大于空气,若装置G用排空气法收集氧气,则气体应从①端通入,将空气排出;检验该装置已经集满氧气的方法是把带火星的木条放到②导气管口,复燃即满;
(4)电石(化学式为CaC2)和水反应乙炔气体(化学式为C2H2),同时生成氢氧化钙,故反应的化学方程式为CaC2+2H2O==Ca(OH)2+C2H2↑;该反应为常温固液反应,故发生装置选C,乙炔密度小于空气,若要制取干燥的气体,应选用向下排空气法进行收集,故收集装置选E,故最合适的装置组合是CE;
(5)A、装置没有进行封闭,将注射器活塞缓缓推进,观察导管口有气泡冒出不能说明整个装置气密性良好,选项错误;B、先将导管插入水中,再用手握住试管,有气泡冒出说明气密性良好,选项正确;C、将注射器缓缓拉动,若观察长颈漏斗下端有气泡冒出则气密性良好,选项正确;D、先将弹簧夹关闭,向长颈漏斗中逐渐加水,若液面不下降说明装置气密性良好,选项正确。故本题选A。

 阅读快车系列答案
阅读快车系列答案【题目】定量研究对于化学科学发展有重大作用,因此我们应该掌握好有关质量守恒定律的相关知识。
(1)下图A、B、C三个实验用于验证质量守恒定律,
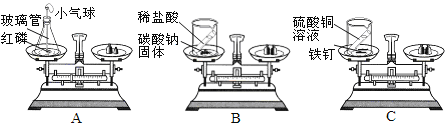
图A中小气球的作用是_________,图C中反应的化学方程式为__________
(2)分别实验后,发现图B不能达到实验目的,原因是___________。
(3)在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 | A | B | C | D |
反应前质量/g | 2 | 24.5 | 4 | 8 |
反应后质量/g | 16.9 | 0 | 13.6 | X |
X的值为______________ ,容器内发生反应的基本类型是_________。