题目内容
【题目】下图是实验室制取气体的一些装置,据图回答有关问题。
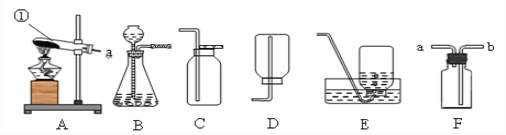
(1)写出指定仪器的名称:①_______。
(2)实验室用双氧水和二氧化锰制取较纯净的氧气装置组合是____,符号表达式为_____________,
(3)写出实验室用高锰酸钾制取氧气的符号表达式是____________________,如果用A作为发生装置,则需改进的是__________________;当选用E装置收集完气体后,测得其纯度明显偏低,原因可能是_______(填序号)
A.高锰酸钾中混入了二氧化锰 B.收集前,集气瓶中未注满水
C.收集后,集气瓶中仍有少量水 D.未见气泡连续均匀冒出时就开始收集
(4)硫化氢(H2S)气体是一种无色有臭鸡蛋气味的气体,密度比空气大,易溶于水,实验室中可以用固体硫化亚铁(FeS)和稀硫酸在常温下反应制取,实验室制取硫化氢气体选用的发生装置为_______(填字母编号);如果用F图所示装置收集硫化氢气体,气体应从______(填“a”或“b”)端管口通入。
(5)在2017年江苏省中学化学创新实验调演中,李彬老师设计了“氢氧焰”的实验,装置如下图所示:
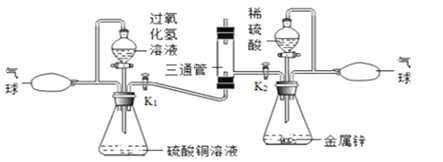
利用氢气与氧气的发生装置制取并储存纯净的气体于气球中。A瓶中硫酸铜溶液的作用是_________,B瓶中产生氢气,通过玻璃活塞K1、K2分别有序控制氧气和氢气的流量,先后进行如下操作:①关闭K2,打开K1,通入氧气,将带火星的木条置于三通管口处,观察到___________,说明氧气具有助燃性。将燃着的木条移开,管口处无火焰。
②关闭K1,打开K2,通入氢气,将燃着的木条置于三通管口处,管口处有火焰。移去燃着的木条,氢气安静地燃烧,说明氢气具有可燃性。把铁片放在火焰上一段时间,铁片呈红热状。打开K1,通入氧气,铁片迅速熔断被切割,由此得出的结沦是_______________________________。
【答案】 试管 BE 略 略 试管口放一团棉花 BD B b 催化作用 木条复燃 氧气含量越高,燃烧就越剧烈
【解析】(1)仪器的名称:①试管。(2)实验室用双氧水和二氧化锰制取较纯净的氧气装置组合是BE,固体与液体反应不需加热制取气体,氧气不易溶于水,符号表达式为∶H2O2 ![]() H2O+O2↑。(3)实验室用高锰酸钾制取氧气的符号表达式是∶KMnO4
H2O+O2↑。(3)实验室用高锰酸钾制取氧气的符号表达式是∶KMnO4 ![]() K2MnO4+MnO2+O2↑,如果用A作为发生装置,则需改进的是试管口放一团棉花;当选用E装置收集完气体后,测得其纯度明显偏低,原因可能是①收集前,集气瓶中未注满水②未见气泡连续均匀冒出时就开始收集。(4)硫化氢(H2S)气体是一种无色有臭鸡蛋气味的气体,密度比空气大,易溶于水,实验室中可以用固体硫化亚铁(FeS)和稀硫酸在常温下反应制取,实验室制取硫化氢气体选用的发生装置为B,固体和液体反应不需加热制取气体;如果用F图所示装置收集硫化氢气体,气体应从b端管口通入,该气体密度比空气大。(5) 利用氢气与氧气的发生装置制取并储存纯净的气体于气球中。A瓶中硫酸铜溶液的作用是催化作用,B瓶中产生氢气,通过玻璃活塞K1、K2分别有序控制氧气和氢气的流量,①关闭K2,打开K1,通入氧气,将带火星的木条置于三通管口处,观察到木条复燃,说明氧气具有助燃性。将燃着的木条移开,管口处无火焰。②关闭K1,打开K2,通入氢气,将燃着的木条置于三通管口处,管口处有火焰。移去燃着的木条,氢气安静地燃烧,说明氢气具有可燃性。把铁片放在火焰上一段时间,铁片呈红热状。打开K1,通入氧气,铁片迅速熔断被切割,由此得出的结沦是①收集前,集气瓶中未注满水②氧气含量越高,燃烧就越剧烈。
K2MnO4+MnO2+O2↑,如果用A作为发生装置,则需改进的是试管口放一团棉花;当选用E装置收集完气体后,测得其纯度明显偏低,原因可能是①收集前,集气瓶中未注满水②未见气泡连续均匀冒出时就开始收集。(4)硫化氢(H2S)气体是一种无色有臭鸡蛋气味的气体,密度比空气大,易溶于水,实验室中可以用固体硫化亚铁(FeS)和稀硫酸在常温下反应制取,实验室制取硫化氢气体选用的发生装置为B,固体和液体反应不需加热制取气体;如果用F图所示装置收集硫化氢气体,气体应从b端管口通入,该气体密度比空气大。(5) 利用氢气与氧气的发生装置制取并储存纯净的气体于气球中。A瓶中硫酸铜溶液的作用是催化作用,B瓶中产生氢气,通过玻璃活塞K1、K2分别有序控制氧气和氢气的流量,①关闭K2,打开K1,通入氧气,将带火星的木条置于三通管口处,观察到木条复燃,说明氧气具有助燃性。将燃着的木条移开,管口处无火焰。②关闭K1,打开K2,通入氢气,将燃着的木条置于三通管口处,管口处有火焰。移去燃着的木条,氢气安静地燃烧,说明氢气具有可燃性。把铁片放在火焰上一段时间,铁片呈红热状。打开K1,通入氧气,铁片迅速熔断被切割,由此得出的结沦是①收集前,集气瓶中未注满水②氧气含量越高,燃烧就越剧烈。
点睛∶根据反应物状态和反应条件选择制气装置,根据气体物理性质溶解性和密度选择收集方法。

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案【题目】某兴趣小组在制取氧气的实验过程中,有如下实验设计方案:
该方案的实验目的是:探究____________________对反应速率的影响。
编号 | 温度 | 催化剂 | 氯酸钾、二氧化锰的质量比 | 生成1升氧气所需时间/s |
实验Ⅰ | 400℃ | MnO2 | 1:1 | 153 |
实验Ⅱ | 400℃ | MnO2 | 2:1 | 240 |
小芳在实验时,误把氧化铜当作二氧化锰放入加热,结果发现也能较快产生氧气,于是进行如下探究:
【猜想Ⅰ】除二氧化锰、氧化铜外,氧化铁(Fe2O3)也可以作氯酸钾分解的催化剂。
【设计实验】
按下表进行实验,并测定开始产生气体时的温度(即分解温度,分解温度越低,表示反应速度越快)。
实验编号 | 实验药品 | 分解温度(℃) |
① | 氯酸钾 | 580 |
② | 氯酸钾和二氧化锰(质量比1︰1) | 350 |
③ | 氯酸钾和氧化铜(质量比1︰1) | 370 |
④ | 氯酸钾和氧化铁(质量比1︰1) | 390 |
【数据和结论】
(1)由实验_________与实验④对比,证明猜想理;
(2)实验所用的三种物质中,催化效果最好的是_____________________。
【反思】
小林在实验时,联想到了渔民用过氧化钙(CaO2)增加鱼池中的含氧量,提出猜想Ⅱ。
【猜想Ⅱ】过氧化钙与水反应可制取氧气。
实验装置 | 实验主要过程 |
| ①检查装置气密性。 ②在试管中加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出。 |
实验结论:过氧化钙与水反应_______(填“能”或“不能”)用于实验室制取氧气。
【分析与反思】
(1)过氧化钙与水反应虽然没有快速收集到大量氧气,但由此实验现象,小林认为渔民用过氧化钙做增氧剂的主要原因是_____________________________。
(2)同学们对过氧化钙与水反应的生成物猜想如下:①氢氧化钙和氧气②碳酸钙和氧气
你认为猜想_______(填序号)一定是错误的,理由是______________________________。
(3)小林希望对此实验进行改进,使该反应加快,请你帮他提出合理化建议_______。
【计算】该兴趣小组的同学们购得用于增氧的过氧化钙产品(杂质不含钙元素),标签如图所示。试计算:

(1)过氧化钙的相对分子质量为_________________;
(2)该产品(右图)中过氧化钙的质量至少为___。



