题目内容
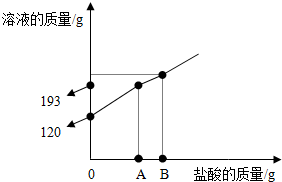 氢氧化钠和碳酸钠的混合物,溶于106.7g水中,形成常温下的不饱和溶液.然后将溶质质量分数为10%的稀盐酸加入到该溶液中,充分反应,反应情况如图所示:
氢氧化钠和碳酸钠的混合物,溶于106.7g水中,形成常温下的不饱和溶液.然后将溶质质量分数为10%的稀盐酸加入到该溶液中,充分反应,反应情况如图所示:(1)A 至B的实验现象
(2)A点时溶液中溶质为
(3)求混合物中氢氧化钠的质量.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:加入稀盐酸时,稀盐酸先和氢氧化钠反应生成氯化钠和水,当氢氧化钠完全反应后,稀盐酸再和碳酸钠反应生成氯化钠、水和二氧化碳;
根据溶液的质量可以计算氢氧化钠和碳酸钠的质量,根据溶液质量差可以计算反应的稀盐酸的质量,进一步可以计算氢氧化钠的质量.
根据溶液的质量可以计算氢氧化钠和碳酸钠的质量,根据溶液质量差可以计算反应的稀盐酸的质量,进一步可以计算氢氧化钠的质量.
解答:解:(1)A点时,稀盐酸和氢氧化钠完全反应,A至B时,稀盐酸和碳酸钠反应,能够观察到产生大量气泡.
故填:产生气泡.
(2)A点时氢氧化钠和稀盐酸完全反应,因此溶液中溶质有反应生成的氯化钠和没有反应的碳酸钠.
故填:氯化钠;碳酸钠.
(3)设氢氧化钠的质量为x,
因为稀盐酸先和氢氧化钠反应,不产生气体和沉淀,所以与氢氧化钠反应的稀盐酸的质量为:193g-120g=73g,
NaOH+HCl═NaCl+H2O,
40 36.5
x 73g×10%
=
,
x=8g,
答:混合物中氢氧化钠的质量是8g.
故填:产生气泡.
(2)A点时氢氧化钠和稀盐酸完全反应,因此溶液中溶质有反应生成的氯化钠和没有反应的碳酸钠.
故填:氯化钠;碳酸钠.
(3)设氢氧化钠的质量为x,
因为稀盐酸先和氢氧化钠反应,不产生气体和沉淀,所以与氢氧化钠反应的稀盐酸的质量为:193g-120g=73g,
NaOH+HCl═NaCl+H2O,
40 36.5
x 73g×10%
| 40 |
| x |
| 36.5 |
| 73g×10% |
x=8g,
答:混合物中氢氧化钠的质量是8g.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
下列化学方程式书写正确的是( )
A、4P+5O2
| ||||
| B、2Fe+6HCl═2FeCl3+3H2↑ | ||||
| C、Fe+CuCl2═FeCl2+Cu↓ | ||||
| D、KMnO4═K2MnO4+MnO2+O2↑ |
把黑色粉末加强热后,有红色物质生成,同时产生一种能使澄清石灰水变浑浊的气体,则该黑色粉末是( )
| A、木炭粉和MnO2 |
| B、CuO |
| C、木炭粉和CuO |
| D、木炭粉 |
在反应2A+2B=2C+D中,C、D的相对分子质量之比为2:3.若4gA与B完全反应后,生成3gD.则在此反应中,B与D的质量比为( )
| A、1:1 | B、2:1 |
| C、5:3 | D、2:3 |

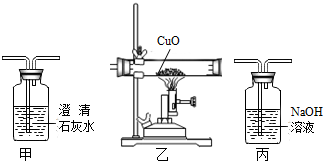
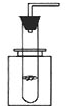 某学生利用一支底部有破损的试管和一个广口瓶组装成制取二氧化碳的发生装置(如图所示),在铜网上应该盛放的是
某学生利用一支底部有破损的试管和一个广口瓶组装成制取二氧化碳的发生装置(如图所示),在铜网上应该盛放的是