题目内容
CO2的制取:
(1)实验室制取CO2的原料是:
(2)有关化学方程式:
(3)收集CO2方法及原理:
(4)
(1)实验室制取CO2的原料是:
(2)有关化学方程式:
(3)收集CO2方法及原理:
(4)
| 鉴定 | 验满 | |
| 二氧化碳 CO2 |
考点:二氧化碳的实验室制法,二氧化碳的检验和验满,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:从二氧化碳的实验制法中的反应原理、收集方法、检验方法和验满方法去分析解答.
解答:解:(1)实验室制取二氧化碳用大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳,故答案为:大理石和稀盐酸;
(2)实验室制取二氧化碳用大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳,其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)二氧化碳气体的密度比空气大、能溶于水,故只能用向上排空气法而不能用排水法,故答案为:向上排水法收集,二氧化碳能溶于水且密度比空气大;
(4)通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成不溶于水的碳酸钙和水;由于二氧化碳的密度比空气大,进入集气瓶后,沉积在集气瓶的底部,二氧化碳自下而上,充满集气瓶,当瓶口有二氧化碳时,说明二氧化碳已收集满,检验二氧化碳是否集满的方法是利用二氧化碳的既不燃烧也不支持燃烧的性质,用燃着的木条放在集气瓶口,如果熄灭,证明集气瓶内已充满二氧化碳;故答案为:通入澄清石灰水,石灰水变浑浊 燃着的木条放在集气瓶口,如果熄灭证明已满.
(2)实验室制取二氧化碳用大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳,其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;故答案为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)二氧化碳气体的密度比空气大、能溶于水,故只能用向上排空气法而不能用排水法,故答案为:向上排水法收集,二氧化碳能溶于水且密度比空气大;
(4)通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成不溶于水的碳酸钙和水;由于二氧化碳的密度比空气大,进入集气瓶后,沉积在集气瓶的底部,二氧化碳自下而上,充满集气瓶,当瓶口有二氧化碳时,说明二氧化碳已收集满,检验二氧化碳是否集满的方法是利用二氧化碳的既不燃烧也不支持燃烧的性质,用燃着的木条放在集气瓶口,如果熄灭,证明集气瓶内已充满二氧化碳;故答案为:通入澄清石灰水,石灰水变浑浊 燃着的木条放在集气瓶口,如果熄灭证明已满.
点评:本题综合性较强,考查学生对实验室制取二氧化碳的反应原理的理解与应用及灵活运用进行分析问题、解决问题的能力.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
在托盘天平两边各放一只等质量的烧杯,在两只烧杯中各加入100g溶质质量分数为7.3%的稀盐酸,将天平调节至平衡,然后向左右两烧杯中加入一定质量的下列各组物质,充分反应后,天平不发生偏转的是( )
| A、5.6g铁粉和5.6g锌粉 |
| B、10g碳酸钙和5.6g氧化钙 |
| C、10g碳酸钙和10.6g碳酸钠 |
| D、2.4g铝和2.4g镁 |
下列是人体中几种体液的正常pH,酸性最强的是( )
| A、胆汁(6.8-7.4) |
| B、唾液(6.6-7.1) |
| C、血液(7.35~7.45) |
| D、胃液(0.8~1.5) |

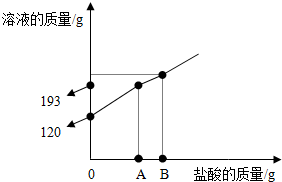 氢氧化钠和碳酸钠的混合物,溶于106.7g水中,形成常温下的不饱和溶液.然后将溶质质量分数为10%的稀盐酸加入到该溶液中,充分反应,反应情况如图所示:
氢氧化钠和碳酸钠的混合物,溶于106.7g水中,形成常温下的不饱和溶液.然后将溶质质量分数为10%的稀盐酸加入到该溶液中,充分反应,反应情况如图所示: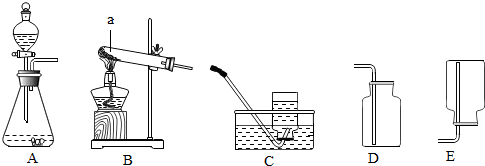
 麻辣小龙虾是一道美食,但有些商贩用“洗虾粉”来清洗龙虾表面的脏,“洗虾粉”中含有草酸,其酸性为醋酸的10000倍,对人体的危害极大.如图为草酸的结构式,试回答下列问题:
麻辣小龙虾是一道美食,但有些商贩用“洗虾粉”来清洗龙虾表面的脏,“洗虾粉”中含有草酸,其酸性为醋酸的10000倍,对人体的危害极大.如图为草酸的结构式,试回答下列问题: