题目内容
【题目】钼(元素符号是Mo)是一种重要的金属,用它制成的合金具有良好的机械性能,在工农业生产和国防上都有着广泛的应用。下图是利用钼矿石(主要成分为MoS2)制备金属钼的流程图,请据图回答下列问题:
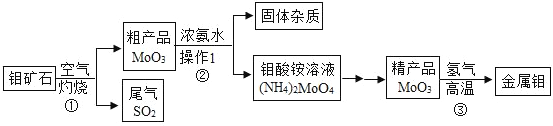
(1)反应①常将钼矿石粉碎,目的是_____。
(2)操作I的名称是_____,所需的玻璃仪器有烧杯、漏斗和_____。
(3)写出反应③的化学方程式:_____。
(4)尾气SO2会对空气造成污染,通常可以用浓氢氧化钠溶液吸收,请写出该反应的化学方程式:_____。
【答案】增大反应物的接触面积,使反应更加充分 过滤 玻璃棒 MoO3+3H2![]() MO+3H2O SO2+2NaOH=Na2SO3+H2O
MO+3H2O SO2+2NaOH=Na2SO3+H2O
【解析】
(1)反应①常将钼矿石粉碎,目的是:增大与空气的接触面积,是其充分反应;
(2)操作I将固体与液体分离的名称是过滤,过滤时所需的玻璃仪器有烧杯、漏斗和玻璃棒(用于引流);
(3)反应③三氧化钼在高温条件下与氢气反应产生钼和水的化学方程式:MoO3+3H2![]() MO+3H2O;
MO+3H2O;
(4)尾气SO2会对空气造成污染,通常可以用浓氢氧化钠溶液吸收,二氧化硫与氢氧化钠反应产生亚硫酸钠和水的化学方程式:SO2+2NaOH=Na2SO3+H2O。

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案【题目】2020年1月25日总建筑面积为3.39万平方米的火神山医院正式开工,火神山医院在建造过程中用到/HDPE膜。HDPE膜具有极好的抗冲击性和防潮性,听完老师的描述后,同学们对HDPE膜的组成元素产生了浓厚的兴趣,进行了如下探究。
(提出问题)HDPE膜由什么元素组成?
(查阅资料)
①HDPE膜能够燃烧,燃烧可能生成一氧化碳。
②碱石灰主要成分是氢氧化钠固体和氧化钙固体。
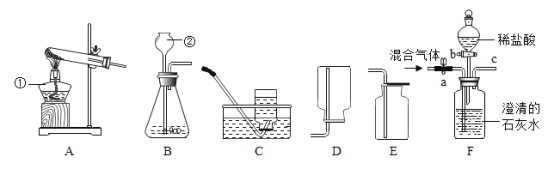
(实验探究)如图所示,先通入干燥氮气,再将4.2g的HDPE膜样品在一定质量的氧气中点燃,并将燃烧产物依次通过装置A、B、C、D (装置中每步反应均进行完全)。
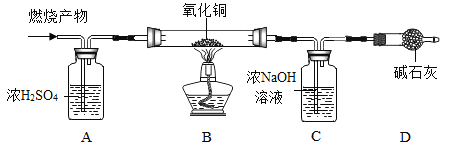
(实验记录)
装置质量 | A装置总质量 | C装置总质量 |
实验前 | 100.0g | 100.0g |
实验后 | 105.4g | 113.2g |
(实验分析)
(1)装置.A中浓硫酸的作用是___________。
(2)当观察到装置B中黑色粉末变成___色,可证明HDPE膜的燃烧产物中有_______。
(3)装置C中发生的化学反应方程式为________________。
(4)装置D的作用是________________。
(实验结论)
HDPE膜由元素_________(填元素符号)组成,它们的原子个数比为______。
(装置优化)
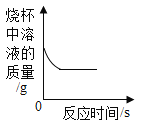
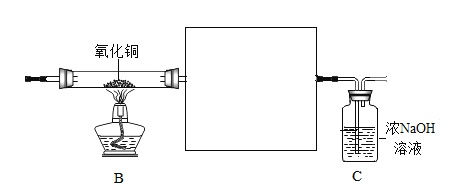
有同学认为,如若操作不当,C中溶液有可能会倒吸回B装置中,使得硬质玻璃管因骤冷而破裂为了降低实验风险,需要进行装置优化,请在方框中画出图像_________。
【题目】已知 KNO3的溶解度如下表所示,下列说法不正确的是
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
A.在 10℃-70℃之间,随着温度的升高,KNO3的溶解度增大
B.20℃时,向 100 g 水中加入 35 g KNO3,充分搅拌,所得溶液质量为 131.6 g
C.将 70℃时不饱和的 KNO3溶液降低温度,有可能转化为饱和溶液
D.50℃时,饱和 KNO3溶液中溶质的质量分数为 85.5%