��Ŀ����
����Ŀ��ˮ����Һ�����ǵ�����ϢϢ��ء�
��1���������е��������ʷ���ˮ�У����γ���Һ����____________________��
A ţ�� B ���� C ��� D ����
��2�������г���_______________��������ˮ��Ӳ�ȣ�����ɱ�����������á�
��3�������·���մ�����ۣ�С���������費Ҫֱ����ˮ��ϴ���������þƾ���ϴ�ྫ��ϴ����ֱ��������ȥ�͵�ԭ��_________________��
��4���ס��ҡ������ֹ������ʵ��ܽ����������ͼ��ʾ���ش��������⣺
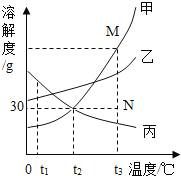
�� �� t2��ʱ���� 30g ���ܽ��� 50gˮ�еõ���Һ������Ϊ_________________
�� ��ͼ�� N ��ļ���Һת��ΪM�ļ���Һ�ķ�����_________________
�� ���ס��ҡ����������ʵı�����Һ�� t3������ t2�������ʵ����������Ĵ�С��ϵ��_________��
�� Ҫ���Ƶ������� t3���ļס��ҡ����������ʵı�����Һ�� ����ˮ��������ϵ��__________�����ƹ���������ȡˮʱ���Ӷ�����������������Һ����������___________������ƫ��������ƫС����
���𰸡�D ��� �ƾ����ܽ����ۡ�ϴ�ྫ���黯 65g ���Ӽ� ���������ˮ ��>��>�� ��>��>�� ƫ��
��������
��1��ţ�������ʲ��ܶ�����ˮ�����Ͳ�������ˮ����۲�������ˮ������������ˮ���������е����ʷ���ˮ�У����γ���Һ���ǰ��ǣ���ѡD��
��2����Ȼˮ���ʱ��ˮ�п����Ըơ�þ������ת��Ϊ������ˮ��Ӳ�Ƚ��͡������г�����з�������ˮ��Ӳ�ȣ�����ɱ�����������ã�
��3�������·���մ�����ۣ�С���������費Ҫֱ����ˮ��ϴ���������þƾ���ϴ�ྫ��ϴ������ȥ�͵�ԭ���ֱ��ǣ��ƾ����ܽ����ۡ�ϴ�ྫ���黯��
(4) ���� t2��ʱ�����ܽ��Ϊ30g�������ܽ�ȸ����֪���� t2��ʱ��50gˮ������ܽ�15g�ף��� 30g���ܽ���50gˮ�еõ���Һ������=50g+15g=65g��
��N��λ�ڼ��ܽ�������·�����t3��ʱ�IJ�������Һ��M��λ�ڼ��ܽ�������ϣ���t3��ʱ�ı�����Һ�����ܽ�����¶ȵ����߶�����ͼ�� N ��ļ���Һת��ΪM�ļ���Һ�ķ��������Ӽ��������ˮ��
�۽�t3��ʱ�ס��ҡ����������ʵı�����Һ���µ�t2��ʱ���ס��ҵ��ܽ�ȼ�С�������ܽ�����¶ȵĽ��Ͷ����ס����о�������������������С��Һ��Ϊ������Һ����û�о��������������������䣬һ���¶��±�����Һ��������������=![]() ���ܽ��Խ����������Խ��t2��ʱ�ҵ��ܽ�ȴ��ڼ��ܽ�ȴ���t3��ʱ�����ܽ�ȡ����Խ��ס��ҡ����������ʵı�����Һ�� t3������ t2�������ʵ����������Ĵ�С��ϵ����>��>����
���ܽ��Խ����������Խ��t2��ʱ�ҵ��ܽ�ȴ��ڼ��ܽ�ȴ���t3��ʱ�����ܽ�ȡ����Խ��ס��ҡ����������ʵı�����Һ�� t3������ t2�������ʵ����������Ĵ�С��ϵ����>��>����
�ܸ����ܽ�����߿�֪��t3��ʱ���ס��ҡ����ܽ�ȱ�<��<�ס��ס��ҡ���Ҫ���Ƶ������� t3���ļס��ҡ����������ʵı�����Һ������ˮ��������ϵ�DZ�>��>�ס����ƹ���������ȡˮʱ���Ӷ�������ȡ��ˮƫС��������������Һ����������ƫ��

 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д� Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�