题目内容
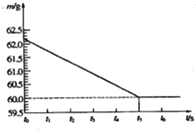
【题目】将碳酸钠和硫酸钠的固体混合物6g放入烧杯中(烧杯质量为20g),再加入36.2g稀硫酸,在一定时间内恰好完全反应,无固体剩余.反应时间(t)和烧杯及其所盛物质的总质量(m)的关系如图所示:
(1)生成气体的质量为 g;6g固体混合物中硫酸钠的质量 g.
(2)所得溶液中溶质的质量分数是 .
【答案】(1)2.2,0.7;(2)19.5%.
【解析】(1)二氧化碳的质量=62.2g﹣60.0g=2.2g;
(2)设原有碳酸钠的质量为x,生成硫酸钠的质量为y,
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 142 44
x y 2.2g
![]() =
=![]() =
=![]()
x=5.3g
y=7.1g
6g固体混合物中硫酸钠的质量是6g﹣5.3g=0.7g;
(3)所得溶液中溶质质量分数为:![]() ×100%=19.5%.
×100%=19.5%.

练习册系列答案
相关题目
